
Effet cocktail : quelle est la toxicité d’un mélange de polluants ?
Pesticides, résidus de médicaments, métaux lourds, composés perfluorés… D’un point de vue strictement écologique, les organismes ne sont pas exposés à une seule substance chimique à un temps donné dans l’environnement, mais le plus souvent à des mélanges complexes de contaminants à plus ou moins à faibles doses. Or, les recherches en écotoxicologie ont montré que la toxicité de ce mélange de substances chimiques était généralement plus élevée que la toxicité individuelle la plus forte (Kortenkam et al., 2009) : on parle d’ « effet cocktail » ou d’« effet combiné ».
1. LES DIFFÉRENTES FORMES D’EFFETS COCKTAIL
La compréhension des effets cocktail est un enjeu de connaissance majeur, pour mieux appréhender les impacts sanitaires et environnementaux des polluants. Le tableau ci-dessous présente les différentes formes d’effets qui peuvent survenir lorsque plusieurs substances chimiques sont présentes en mélange.
| EFFET | DÉFINITION | TRADUCTION MATHÉMATIQUE | INTERACTION ENTRE LES SUBSTANCES CHIMIQUES |
| ADDITION (ou « additivité ») | C’est lorsque l’effet combiné de plusieurs substances chimiques est égal à la somme des effets de chaque substance | 1 + 2 = 3 | Aucune interaction |
| SYNERGIE (ou « supra-additivité ») | Phénomène par lequel plusieurs substances chimiques agissant ensemble créent un effet plus grand que la somme des effets individuels | 1 + 2 = 5 | Interaction avec augmentation de l’effet |
| POTENTIALISATION | C’est lorsqu’une substance non toxique augmente la toxicité d’une autre substance chimique | 0 + 3 = 5 | Interaction avec augmentation de l’effet |
| ANTAGONISME (ou « Infra-additivité ») | C’est lorsque l’effet combiné de plusieurs substances chimiques est inférieur à la somme des effets de chaque substance | 1 + 3 = 2 | Interaction avec diminution de l’effet |
2. L’ADDITIVITÉ EST LE CAS LE PLUS FRÉQUENT
La plupart des scientifiques ayant travaillé sur les interactions toxicologiques ou écotoxicologiques s’accordent à penser que l’additivité́ est le phénomène se produisant dans la majorité des cas (Badot, 2011 ; Kortenkam et al., 2009 ; Ribera et Taberly, 2011). En d’autres termes, la toxicité/réponse d’un mélange de substances sera égale approximativement à la somme des toxicités/réponses individuelles des substances prises séparément. On parle de non interaction entre les polluants. Ces substances ont alors dans le plus grand cas de figure un modèle d’action indépendante c’est-à-dire qu’elles agissent sur différents systèmes et produisent des effets qui ne s’influencent pas.
Cependant, les effets des substances chimiques présentes en mélange ne sont pas toujours additifs. Dans ces situations qui représenteraient 20 à 40 % des cas (Jonker et al., 2004), la somme des effets individuels des substances (« co-contaminants ») pris isolément peut être supérieure au résultat attendu (on parle de « synergie ») ou inférieur au résultat attendu (on parle d’ « antagonisme »).
La potentialisation est un autre cas de figure. Une substance A qui, prise isolément, n’engendre aucune réponse, peut, en présence d’une autre substance B, augmenter la réponse de cette dernière, excédant ainsi la somme des deux réponses individuelles. Synergie, antagonisme et potentialisation résultent tous les trois d’interactions entre les effets des substances chimiques.
3. PLUSIEURS FACTEURS INFLUENCENT CES EFFETS COCKTAIL
L’existence d’interactions entre les substances chimiques présentes dans un mélange ne dépend pas seulement de la dose ou de la concentration d’exposition. D’autres facteurs peuvent intervenir comme par exemple :
- Les conditions du milieu (température, pH, etc.)
- La proportion respective de chaque substance dans le mélange (ratios de doses ou de concentrations) ;
- L’ordre dans lequel des substances sont introduites ;
- La fréquence d’exposition ;
- Les caractéristiques individuelles des organismes exposés (patrimoine génétique, différences entre espèces, différences associées à l’âge, etc.).
4. QUELQUES EXEMPLES D’EFFETS COCKTAIL
4.1 Métabolisme du malathion en absence ou en présence d’autres substances chimiques
L’interaction entre plusieurs contaminants chimiques peut être liée à l’inhibition d’une substance par une autre ou à l’augmentation de son activation métabolique, la rendant plus toxique (synergie, potentialisation).
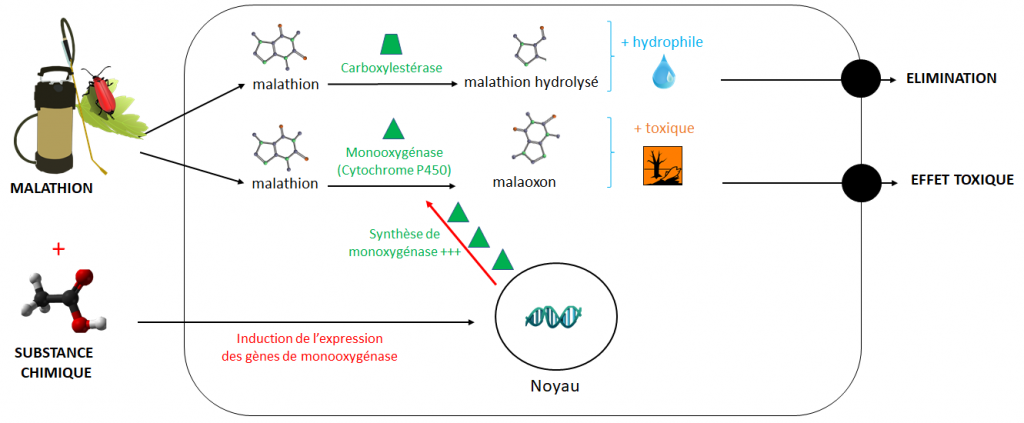
Par exemple, au sein d’un organisme, le malathion, insecticide organophosphoré (voir Figure 1) :
- est détoxifié (= rendu moins toxique) par l’action d’une première enzyme appelée carboxylestérase* : cette dernière hydrolyse (« casse ») le malathion qui peut ainsi être plus facilement éliminé par l’organisme ;
- est activé (= rendu plus toxique) par une seconde enzyme appelée monooxygénase** : cette dernière transforme le malathion en malaoxon, qui est plus toxique que sa molécule mère.
La toxicité du malathion dépendra donc de l’importance relative de ces deux enzymes concurrentes. De fait, si des substances chimiques capables d’induire la production (synthèse) de monooxygénases sont présentes dans un mélange, elles peuvent rendre le malathion plus toxique en favorisant l’activation de ce dernier.
4.2 Liaisons entre des métaux et des protéines
Les métallothionéines sont des protéines présentes chez tous les animaux. Elles jouent un rôle majeur en régulant la concentration des métaux essentiels à l’organisme comme le cuivre et le zinc. Elles ont également la capacité de se lier à des métaux lourds non essentiels (plomb, mercure, cadmium, etc.), contribuant à la réduction de leur effet toxique et à leur élimination.
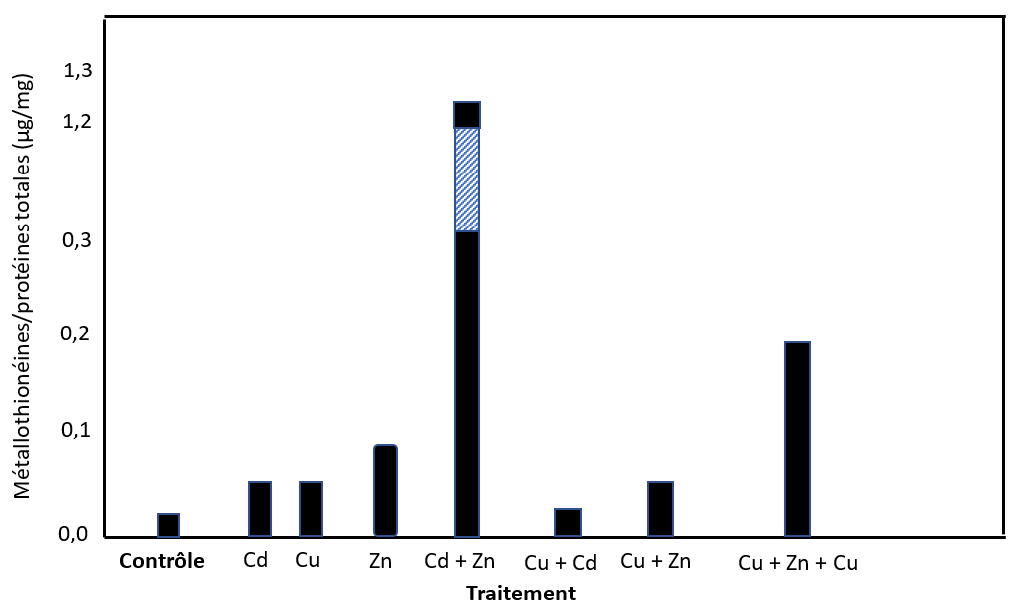
La régulation de l’expression des gènes à l’origine de la synthèse (production) de ces métallothionéines a fait l’objet de nombreuses recherches. Des travaux ont ainsi étudié l’influence de la présence d’un ou plusieurs métaux sur l’induction de cette expression génique chez le crabe (Forbes et al, 2006). Leurs résultats, présentés sur la figure 2, montre que l’effet combiné peut être très différent selon le mélange de métaux concerné :
- en présence de « cadmium + cuivre » ou de « zinc + cuivre », l’expression des gènes de métallothioniéines est inférieure à la somme des expressions induites par chacun de ces métaux, mesurées séparément : ce résultat illustre le phénomène d’antagonisme ;
- en présence de « cadmium + zinc », l’expression est largement supérieure à la somme des effets individuels des métaux pris séparément : ce résultat illustre le phénomène de synergie ;
- en présence de « cadmium + zinc + cuivre », l’expression est égale à la somme des effets individuels des métaux pris séparément : ce résultat illustre le phénomène d’additivité.
4.3 L’effet combiné d’un insecticide et d’un fongicide sur les abeilles
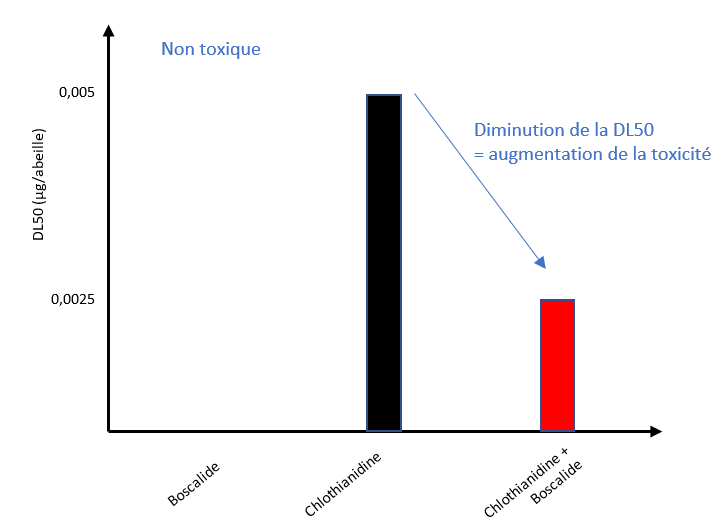
Illustrons maintenant le phénomène de potentialisation. Le boscalide, qui est un fongicide, est sans effet sur la mortalité des abeilles lorsqu’il est appliqué seul. Il a pourtant la propriété, lorsqu’il est appliqué en mélange avec des néonicotinoïdes (classe d’insecticides agissant sur le système nerveux des insectes) tels que la chlothianidine, d’augmenter significativement leur effet létal chez les abeilles mellifères, en diminuant la dose entrainant une mortalité de 50 % des abeilles (DL50) (Figure 3) (Tsvetkov et al. 2017).
5. LA RÉGLEMENTATION NE PREND PAS EN COMPTE CES EFFETS COCKTAIL
5.1 L’évaluation a priori est faite substance par substance
Presque toute la toxicité réglementaire (réalisée à l’aide de bioessais) est effectuée en évaluant la réponse ou la toxicité de chacune des substances prises isolément. C’est le cas notamment de la réglementation REACH, qui contraint les industriels à évaluer la toxicité des substances mises sur le marché européen (substances produites ou importées en quantité supérieure à 1 tonne/an).
Cette méthodologie ne permet pas de connaître les réponses lorsque les cellules/organismes sont exposés à plusieurs substances chimiques simultanément, et ne prend donc pas en compte la synergie possible entre la substance testée et les autres contaminants présents dans l’environnement.
5.2 L’évaluation a posteriori (in situ) est le plus souvent basée sur des mesures chimiques
Cette non prise en compte des effets cocktail par la réglementation est également vraie pour l’évaluation in situ, dans le milieu naturel. Par exemple, les analyses réglementaires réalisées pour évaluer l’état d’une rivière au titre de la Directive européenne cadre sur l’eau sont basées sur la mesure de concentrations unitaires de quelques dizaines de substances chimiques, comparées à des valeurs seuils déterminées préalablement via des bioessais de laboratoire. Ces mesures ne permettent donc pas d’évaluer les potentiels effets toxiques du mélange de polluants.
A l’opposé, la biosurveillance, qui repose sur l’évaluation des effets mesurés sur des organismes vivants prélevés ou encagés dans le milieu naturel, est une approche très prometteuse pour évaluer des effets des cocktails de polluants présents dans l’environnement. Développée à partir des années 1980, elle est encore peu reconnue par la réglementation mais trouve peu à peu sa place dans les réseaux de surveillance, notamment dans le milieu aquatique.
Lire aussi | Évaluer les effets des polluants chimiques sur les êtres vivants et les écosystèmes
6. COMMENT ÉVALUER CES EFFETS COCKTAIL ?
Le modèle des unités toxiques est une des approches d’analyse des effets des mélanges de substances chimiques, développée à la fin des années 1960 (Rivera et Taberly, 2011).
Une unité toxique (UT) est définie comme étant la concentration d’une substance dans un mélange, divisée par sa concentration toxique individuelle relative à un effet donné (ex. : immobilisation, mortalité, etc.) sur un organisme étudié (ex. la daphnie). Cette concentration toxique est généralement exprimée via une CE50 (concentration efficace qui engendre un effet de 50 % par rapport au témoin) ou une CL50 (concentration engendrant une mortalité de 50 % des individus).
Le calcul de l’unité toxique d’une substance i présente dans un mélange, se fait via l’équation suivante :

La somme des unités toxiques de chacune des substances présentes dans le mélange permet de qualifier l’effet combiné de ce mélange :
- si la somme des unités toxiques de chaque substance du mélange est approximativement égale à 1 (∑ UT ≈ 1), alors il y a additivité ;
- si la somme est inférieure à 1 (∑ UT < 1), alors il y a antagonisme ;
- si la somme est supérieure à 1 (∑ UT > 1), alors il y a synergie ;
Bien que ce type d’approche soit très utile pour évaluer ces effets cocktails, tester la toxicité d’une proportion significative de combinaisons chimiques présentes dans les écosystèmes terrestres, marins ou d’eau douce est malheureusement peu réalisable. En effet, si l’on prend le cas de 10 substances chimiques, il faudrait tester plus de mille combinaisons de mélange !
7. CONCLUSION
Les organismes vivants sont exposés dans l’environnement à des mélanges de polluants et des questions se posent sur des possibles interactions entre les composants de ces mélanges. Quand les substances chimiques sont testées à l’aide de bioessais, elles le sont généralement individuellement. Dans un certain nombre de cas, la toxicité de mélanges est plus élevée qu’un effet additif. Une meilleure connaissance de la toxicologie biochimique des polluants permettra de prédire les interactions entre polluants.
Certaines des substances chimiques qui, prises isolément, s’avèrent sans danger, peuvent devenir nocives lorsqu’elles sont combinées à d’autres substances. Il existe effectivement dans notre environnement plus de 100 000 substances chimiques dont l’action combinée pourrait avoir des effets inattendus sur les organismes au regard de leur innocuité reconnue ou supposée en tant que substances isolées. Si ces travaux sont confirmés in vivo, des retombées importantes sont attendues dans les domaines de l’écotoxicologie et de l’évaluation des risques liés à l’utilisation des produits chimiques.

Article posté le 1er décembre 2023 par Dorothée Rivet, responsable de l’UE d’écotoxicologie en L3 à l’Université Sorbonne Paris Nord de 2013 à 2023 et co-autrice du livre Ecotoxicologie paru en 2022 chez Dunod
*La carboxylestérase est une enzyme de type hydrolase qui peut jouer un rôle dans la biotransformation des esters (comme le malathion) selon la réaction suivante R-COOHR’ + H2O en R-COOH + R’OH.
**Les monooxygénases sont des enzymes qui incorporent un groupe hydroxyle dans un substrat dans de nombreuses voies métaboliques. Les monooxygénases les plus importantes sont les cytochromes P450 (CYP), qui sont impliquées, entre autres, dans le métabolisme de plusieurs produits chimiques dans le corps, dont des polluants organiques.
| Vous avez apprécié cet article ? Soutenez Ecotoxicologie.fr et contribuez à son développement avec petit don 🙂 |







 Il se vend près de 6 shampoings chaque seconde en France soit près de 200 millions de bouteilles par an
Il se vend près de 6 shampoings chaque seconde en France soit près de 200 millions de bouteilles par an Les produits d’entretien classiques contiennent des tensioactifs (appelés aussi agents de surface ou détergents) qui permettent d’éliminer les graisses et autres salissures à la surface de matériaux. Les détergents anioniques (charge négative) et amphotériques (dont la charge dépend du pH de l’eau) sont particulièrement présents dans les produits nettoyants, en raison de leurs propriétés nettoyantes et moussantes
Les produits d’entretien classiques contiennent des tensioactifs (appelés aussi agents de surface ou détergents) qui permettent d’éliminer les graisses et autres salissures à la surface de matériaux. Les détergents anioniques (charge négative) et amphotériques (dont la charge dépend du pH de l’eau) sont particulièrement présents dans les produits nettoyants, en raison de leurs propriétés nettoyantes et moussantes  Les phtalates, produits à quelque 6 millions de tonnes par an dans le monde
Les phtalates, produits à quelque 6 millions de tonnes par an dans le monde  20 millions de lave-linge tournent en France chaque jour en moyenne
20 millions de lave-linge tournent en France chaque jour en moyenne  La France est le 4ème consommateur mondial de médicaments : plus de 3000 médicaments à usage humain et 300 médicaments vétérinaires sont actuellement disponibles sur le marché français. Une fois que ces substances ont agi dans l’organisme, elles sont excrétées, essentiellement dans les selles et les urines, puis relarguées dans les réseaux d’eaux usées (médicaments humains) et dans les sols (médicaments vétérinaires). Une partie de ces résidus de médicaments se retrouvent donc d’une manière ou d’une autre dans le milieu aquatique. Des traces de ces composés sont d’ailleurs régulièrement détectées dans les eaux de surface et même dans les eaux de nappe
La France est le 4ème consommateur mondial de médicaments : plus de 3000 médicaments à usage humain et 300 médicaments vétérinaires sont actuellement disponibles sur le marché français. Une fois que ces substances ont agi dans l’organisme, elles sont excrétées, essentiellement dans les selles et les urines, puis relarguées dans les réseaux d’eaux usées (médicaments humains) et dans les sols (médicaments vétérinaires). Une partie de ces résidus de médicaments se retrouvent donc d’une manière ou d’une autre dans le milieu aquatique. Des traces de ces composés sont d’ailleurs régulièrement détectées dans les eaux de surface et même dans les eaux de nappe  On estime que 4000 à 6000 tonnes d’écran total sont libérées chaque année dans les zones de récifs tropicales par les 78 millions de touristes qui s’y rendent
On estime que 4000 à 6000 tonnes d’écran total sont libérées chaque année dans les zones de récifs tropicales par les 78 millions de touristes qui s’y rendent  En raison de son faible coût, l’huile de palme est, depuis quelques années, très utilisée dans l’alimentation: elle est présente dans 1 produit alimentaire empaqueté sur deux vendus en Europe (chips, biscuits, crème glacée, etc.). Or, la plantation de palmiers est à l’origine de déforestation, notamment en Indonésie. Dans ce pays, 3 millions d’hectares de forêt tropicale ont été détruits à cet effet entre 1990 et 2005 et le gouvernement prévoit un plan d’expansion des plantations de palmiers à huile de 14 millions d’hectares. La conversion des forêts en palmiers à huile a montré une perte de 80 à 100% des espèces de mammifères (dont l’orang-outan), reptiles et d’oiseaux dans ces zones
En raison de son faible coût, l’huile de palme est, depuis quelques années, très utilisée dans l’alimentation: elle est présente dans 1 produit alimentaire empaqueté sur deux vendus en Europe (chips, biscuits, crème glacée, etc.). Or, la plantation de palmiers est à l’origine de déforestation, notamment en Indonésie. Dans ce pays, 3 millions d’hectares de forêt tropicale ont été détruits à cet effet entre 1990 et 2005 et le gouvernement prévoit un plan d’expansion des plantations de palmiers à huile de 14 millions d’hectares. La conversion des forêts en palmiers à huile a montré une perte de 80 à 100% des espèces de mammifères (dont l’orang-outan), reptiles et d’oiseaux dans ces zones  Les animaux se nourrissent d’aliments (céréales, petits animaux, etc.) contenant différents polluants. Au fil du temps, ces derniers s’accumulent dans l’organisme de l’animal et en particulier dans les graisses (phénomène de bioaccumulation). Ainsi, une étude de 2010 a révélé la présence de nombreux pesticides et de PCB dans du saumon et du steak haché achetés dans des supermarchés de la région parisienne
Les animaux se nourrissent d’aliments (céréales, petits animaux, etc.) contenant différents polluants. Au fil du temps, ces derniers s’accumulent dans l’organisme de l’animal et en particulier dans les graisses (phénomène de bioaccumulation). Ainsi, une étude de 2010 a révélé la présence de nombreux pesticides et de PCB dans du saumon et du steak haché achetés dans des supermarchés de la région parisienne  Tout comme les fruits et légumes, le riz peut contenir différents polluants tels que des pesticides, en particulier s’il est issu d’une agriculture intensive classique (non « bio »). Ainsi, une étude de 2010 a révélé la présence d’isoprothiolane et de tricyclazole, 2 pesticides interdits d’usage en Europe, dans du riz acheté dans des supermarchés de la région parisienne
Tout comme les fruits et légumes, le riz peut contenir différents polluants tels que des pesticides, en particulier s’il est issu d’une agriculture intensive classique (non « bio »). Ainsi, une étude de 2010 a révélé la présence d’isoprothiolane et de tricyclazole, 2 pesticides interdits d’usage en Europe, dans du riz acheté dans des supermarchés de la région parisienne  L’eau du robinet est globalement de bonne qualité en France et les normes en vigueur sont généralement respectées
L’eau du robinet est globalement de bonne qualité en France et les normes en vigueur sont généralement respectées  Les fruits et légumes issus de l’agriculture intensive « classique » (c’est à dire non « bio ») contiennent des mélanges à faibles doses de substances chimiques classées, par les instances officielles, cancérogènes certaines, probables ou possibles ou soupçonnées d’être perturbatrices du système endocrinien. C’est ce qu’illustre notamment une étude de 2010 qui a révélé la présence de nombreux pesticides dans des produits achetés dans des supermarchés de la région parisienne
Les fruits et légumes issus de l’agriculture intensive « classique » (c’est à dire non « bio ») contiennent des mélanges à faibles doses de substances chimiques classées, par les instances officielles, cancérogènes certaines, probables ou possibles ou soupçonnées d’être perturbatrices du système endocrinien. C’est ce qu’illustre notamment une étude de 2010 qui a révélé la présence de nombreux pesticides dans des produits achetés dans des supermarchés de la région parisienne  Le lave-vaisselle est généralement moins consommateur en eau (12 L) que le lavage à la main qui dépend beaucoup du manipulateur (10 à 50 L)
Le lave-vaisselle est généralement moins consommateur en eau (12 L) que le lavage à la main qui dépend beaucoup du manipulateur (10 à 50 L)  Le liquide vaisselle est un détergent composé d’agents nettoyants appelés tensioactifs, mais aussi de colorants, conservateurs et parfums de synthèse. Bien que les tensioactifs ont l’obligation d’être biodégradables à 90%
Le liquide vaisselle est un détergent composé d’agents nettoyants appelés tensioactifs, mais aussi de colorants, conservateurs et parfums de synthèse. Bien que les tensioactifs ont l’obligation d’être biodégradables à 90%  Les composés perfluorés (PFC), tels que le téflon, ont la propriété de repousser l’eau, les matières grasses et la poussière. Ils sont ainsi utilisés comme antiadhésif dans de nombreuses poêles et casseroles. Les PFC sont persistants et s’accumulent dans les êtres vivants: certaines études ont révélé la présence de certains PFC dans les cours d’eau et les poissons (dans le foie notamment) ainsi que dans le sang humain
Les composés perfluorés (PFC), tels que le téflon, ont la propriété de repousser l’eau, les matières grasses et la poussière. Ils sont ainsi utilisés comme antiadhésif dans de nombreuses poêles et casseroles. Les PFC sont persistants et s’accumulent dans les êtres vivants: certaines études ont révélé la présence de certains PFC dans les cours d’eau et les poissons (dans le foie notamment) ainsi que dans le sang humain  3,8 millions de tonnes de bisphénol A (BPA) ont été produits en 2006
3,8 millions de tonnes de bisphénol A (BPA) ont été produits en 2006  Ces bouteilles contiennent notamment des phtalates, produits chimiques utilisés en tant que plastifiants et qui font partie de la famille des
Ces bouteilles contiennent notamment des phtalates, produits chimiques utilisés en tant que plastifiants et qui font partie de la famille des
2 commentaires
Ping :
Ping :