
« Les pluies acides » : acidification des eaux de surface

Regardez ces rivières des Vosges ! Au premier coup d’œil, on voit de l’eau pure, un espace de nature préservée de toute pollution, un refuge pour de nombreuses espèces animales…
Et pourtant, on aurait tort de s’arrêter à ces premières impressions !
Ce sont au contraire des cours d’eau extrêmement pollués et très pauvres en biodiversité ! Ces rivières sont en effet soumises à une pollution peu visible mais pourtant bien réelle : l’acidification des eaux.
I. COMMENT LES EAUX DE SURFACE SONT-ELLES ACIDIFIÉES ?
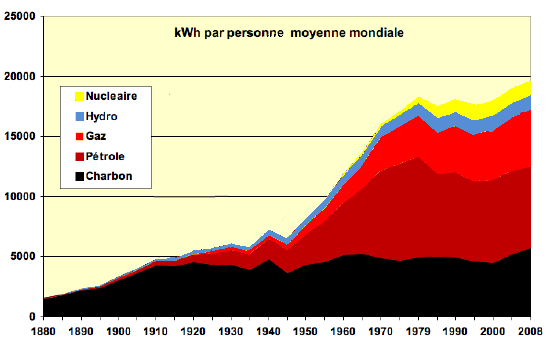
Depuis la fin du XIXème siècle et la révolution industrielle, la consommation d’énergies fossiles (charbon, pétrole et gaz) n’a cessé d’augmenter.
Cette combustion d’énergies fossiles a pour conséquence des émissions dans l’atmosphère :
- de SO2 (dioxyde de soufre) : pour la production d’énergie électrique, dans les industries et les transports
- de NOx (oxydes d’azotes NO et NO2) : pour la production d’énergie électrique, les transport et l’agriculture
Ces composés sont ensuite transportés par les masses d’air. Une partie subit alors des transformations chimiques : des composés que l’on nomme « acides forts » sont formés.
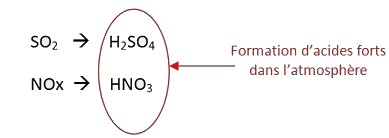
Par la suite, les polluants se déposent, souvent très loin de leurs lieux d’émissions. Par exemple, différentes études ont montré que l’émission de polluants en Allemagne donnait lieu à des dépôts dans certains cours d’eau des Vosges, en France.
Deux types de dépôts sont observés :
- les dépôts humides : H2SO4 et HNO3 (acides issus des transformations de l’atmosphère) sont déposés au sol par les précipitations (pluies, neiges, brouillard). On appelle plus communément ces dépôts, des pluies acides. Ce terme est plutôt mal choisi car les pluies sont naturellement acides (pH d’environ 5,4 à 5,6 donc inférieur à pH 7, le pH neutre). Cependant les « pluies acides » ont une acidité encore plus importante, due aux polluants (acides forts) qu’elles contiennent. Dans les Vosges, un pH d’environ 4,5 a ainsi été mesuré dans l’eau de pluie (Collin, 1989).
- les dépôts secs : SO2 et NOx sont déposés sous la forme de particules, sels ou gaz. Ils sont alors transformés en H2SO4 et HNO3 au contact de l’humidité.
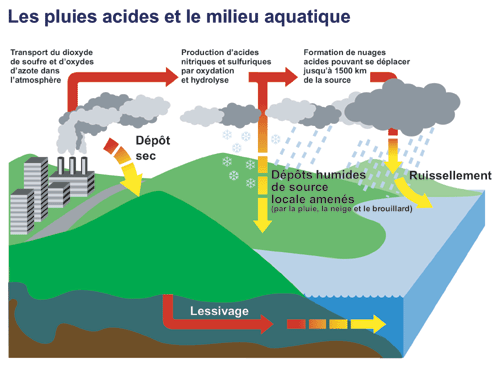
Ces dépôts sont à l’origine de l’acidification des eaux de surface. En effet, ils peuvent acidifier progressivement les sols. Dans un premier temps, le sol joue un rôle de tampon : il parvient à « absorber » ces dépôts acides. Cependant, ce pouvoir tampon est moins efficace dans le cas où la roche mère (roche présente sous le sol) est pauvre et difficilement altérable (ex : granite). Dans ce cas, si ces dépôts perdurent, ils parviennent à acidifier durablement les sols.
La végétation joue également un rôle dans l’acidification des eaux. En effet, les arbres constituent un filtre de la basse atmosphère, en raison de leur grande taille. Les dépôts atmosphériques sont ainsi plus élevés en forêt qu’en zone découverte. Les conifères sont les arbres captant le plus de dépôts atmosphériques car ils gardent leur feuillage toute l’année.
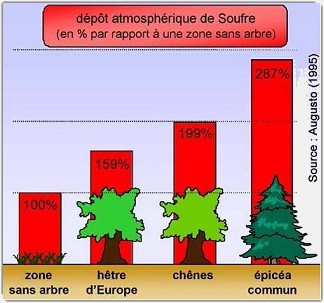
Lors de précipitations, les composés acides peuvent alors atteindre les eaux de surface, par infiltration ou ruissellement.
En résumé :
DÉPÔTS ACIDES + ROCHE PAUVRE ET FACILEMENT ALTÉRABLE + CONIFÈRES = ACIDIFICATION DES EAUX
II. QU’EST-CE QU’UN COURS D’EAU (OU LAC) ACIDIFIÉ ?
Un cours d’eau acidifié possède un pH très bas en comparaison des autres cours d’eau. Pour rappel, un pH bas correspond à une forte concentration en ions H+, ces ions H+ provenant des dépôts acides dont on a parlé précédemment. Il présente également des teneurs en aluminium souvent élevées et des teneurs en calcium et magnésium souvent faibles, dues aux échanges au niveau des sols.
Il existe des cours d’eau et des lacs acides dans différents pays de l’hémisphère nord : États-Unis, Canada, Norvège, Suède, Allemagne, Russie, France, etc.
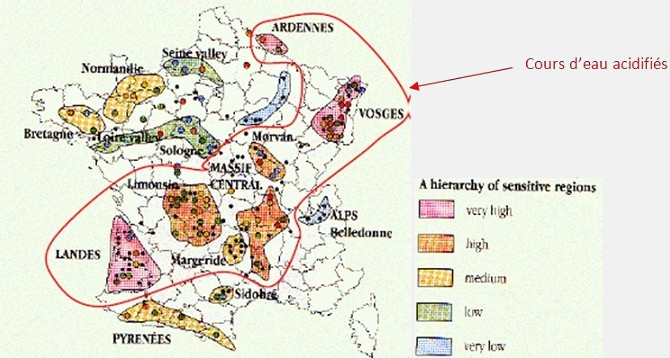
III. QUELS SONT LES EFFETS DE L’ACIDIFICATION DES EAUX DE SURFACE ?
L’acidification des eaux provoque une érosion de la biodiversité
L’indice de Shannon (H’) permet d’évaluer la biodiversité au sein d’un milieu. Plus la valeur de cet indice est élevée et plus la biodiversité est importante.
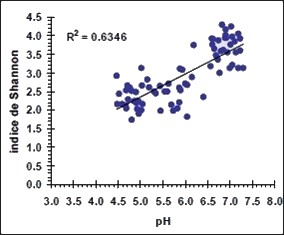
L’indice de Shannon (H’) permet d’évaluer la biodiversité au sein d’un milieu. Plus la valeur de cet indice est élevée et plus la biodiversité est importante.
Le graphique ci-contre présente l’indice de Shannon appliqué aux macro-invertébrés benthiques (invertébrés vivants au fond des cours d’eau) en fonction de l’acidité d’un cours d’eau. On voit ici que plus le pH du cours d’eau diminue et plus la biodiversité est faible (Gerold, 2010).
De même, plus la concentration en Aluminium augmente et plus cette biodiversité diminue. Enfin, lorsque la concentration en Calcium ou Magnésium diminue et plus cette biodiversité diminue.
Un cours d’eau ou un lac acidifié présentent donc une diversité biologique faible.
D’où vient cette perte de biodiversité ?
Certaines espèces ne peuvent pas vivre dans de l’eau trop acide : on les qualifie d’acido-sensibles. Lorsqu’un cours d’eau est acidifié on a donc une disparition de certaines espèces. C’est le cas, par exemple, de la truite fario, sensible à l’acidification et qui a disparu de nombreux cours d’eau acidifiés des Vosges. Cette sensibilité s’explique par les modifications des concentrations en ions H+, aluminium, calcium et magnésium dans les cours d’eau acides, qui affectent ces organismes.
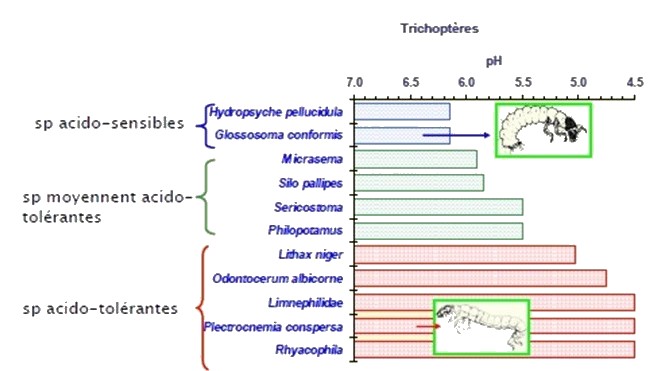

L’acidification des cours d’eau a également un effet sur l’ensemble de la chaîne alimentaire. En effet, dans un cours d’eau acidifié, l’activité de certains champignons microscopiques (hyphomycètes) diminue.
Or, ces champignons dégradent les feuilles mortes qui se déposent dans les cours d’eau. En cas d’acidification, cette fonction de dégradation des feuilles mortes n’est plus assurée. Certains organismes ne sont capables de se nourrir de ces feuilles, que si elles sont dégradés (les déchiqueteurs, puis les collecteurs). Le nombre de ces organismes aura donc tendance à diminuer dans un cours d’eau acidifié. De même, les prédateurs de ces organismes (notamment des poissons), perdront une source de nourriture et verront leurs effectifs diminuer.
IV. QUEL AVENIR POUR CES ÉCOSYSTÈMES ?
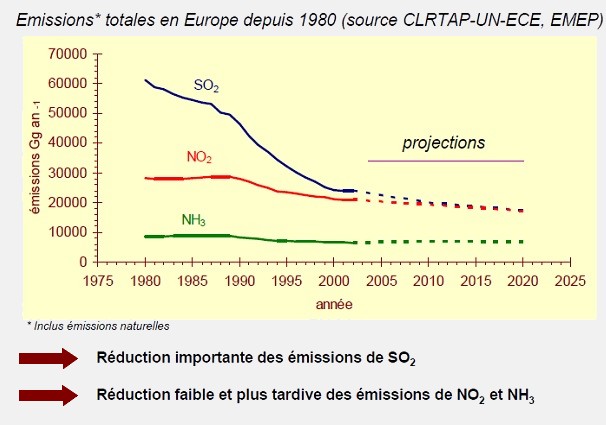
Vers une diminution globale des émissions de polluants responsables des dépôts acides
Face aux nombreux problèmes de dégradations des écosystèmes à travers l’hémisphère nord, différents protocoles ont été ratifiés pour réduire les émissions des polluants à l’origine de ces dépôts acides. Globalement, les émissions de ces polluants ont diminué même si ce n’est pas le cas dans toutes les régions du monde. Cependant, de nombreux cours d’eau et lacs sont aujourd’hui encore acidifiés (notamment dans les Vosges), et cela malgré la diminution des émissions de SO2 et NOx.
Vers une adaptation de certaines espèces ?
La truite ayant disparu de certains cours d’eau acidifiés des Vosges, des associations de pêcheurs organisent des lâchers de truites réguliers. Or, au fil des années, certaines de ces truites ont développé une forme de résistance à l’acidification, qu’elles ont transmis à leur descendance.
Article rédigé par Vivien Lecomte, 3 janvier 2012 – Ecotoxicologie.fr
| Ecotoxicologie.fr est entièrement gratuit et sans publicité… mais produire du contenu a un coût : soutenez-nous 🙂 |






 Il se vend près de 6 shampoings chaque seconde en France soit près de 200 millions de bouteilles par an
Il se vend près de 6 shampoings chaque seconde en France soit près de 200 millions de bouteilles par an Les produits d’entretien classiques contiennent des tensioactifs (appelés aussi agents de surface ou détergents) qui permettent d’éliminer les graisses et autres salissures à la surface de matériaux. Les détergents anioniques (charge négative) et amphotériques (dont la charge dépend du pH de l’eau) sont particulièrement présents dans les produits nettoyants, en raison de leurs propriétés nettoyantes et moussantes
Les produits d’entretien classiques contiennent des tensioactifs (appelés aussi agents de surface ou détergents) qui permettent d’éliminer les graisses et autres salissures à la surface de matériaux. Les détergents anioniques (charge négative) et amphotériques (dont la charge dépend du pH de l’eau) sont particulièrement présents dans les produits nettoyants, en raison de leurs propriétés nettoyantes et moussantes  Les phtalates, produits à quelque 6 millions de tonnes par an dans le monde
Les phtalates, produits à quelque 6 millions de tonnes par an dans le monde  20 millions de lave-linge tournent en France chaque jour en moyenne
20 millions de lave-linge tournent en France chaque jour en moyenne  La France est le 4ème consommateur mondial de médicaments : plus de 3000 médicaments à usage humain et 300 médicaments vétérinaires sont actuellement disponibles sur le marché français. Une fois que ces substances ont agi dans l’organisme, elles sont excrétées, essentiellement dans les selles et les urines, puis relarguées dans les réseaux d’eaux usées (médicaments humains) et dans les sols (médicaments vétérinaires). Une partie de ces résidus de médicaments se retrouvent donc d’une manière ou d’une autre dans le milieu aquatique. Des traces de ces composés sont d’ailleurs régulièrement détectées dans les eaux de surface et même dans les eaux de nappe
La France est le 4ème consommateur mondial de médicaments : plus de 3000 médicaments à usage humain et 300 médicaments vétérinaires sont actuellement disponibles sur le marché français. Une fois que ces substances ont agi dans l’organisme, elles sont excrétées, essentiellement dans les selles et les urines, puis relarguées dans les réseaux d’eaux usées (médicaments humains) et dans les sols (médicaments vétérinaires). Une partie de ces résidus de médicaments se retrouvent donc d’une manière ou d’une autre dans le milieu aquatique. Des traces de ces composés sont d’ailleurs régulièrement détectées dans les eaux de surface et même dans les eaux de nappe  On estime que 4000 à 6000 tonnes d’écran total sont libérées chaque année dans les zones de récifs tropicales par les 78 millions de touristes qui s’y rendent
On estime que 4000 à 6000 tonnes d’écran total sont libérées chaque année dans les zones de récifs tropicales par les 78 millions de touristes qui s’y rendent  En raison de son faible coût, l’huile de palme est, depuis quelques années, très utilisée dans l’alimentation: elle est présente dans 1 produit alimentaire empaqueté sur deux vendus en Europe (chips, biscuits, crème glacée, etc.). Or, la plantation de palmiers est à l’origine de déforestation, notamment en Indonésie. Dans ce pays, 3 millions d’hectares de forêt tropicale ont été détruits à cet effet entre 1990 et 2005 et le gouvernement prévoit un plan d’expansion des plantations de palmiers à huile de 14 millions d’hectares. La conversion des forêts en palmiers à huile a montré une perte de 80 à 100% des espèces de mammifères (dont l’orang-outan), reptiles et d’oiseaux dans ces zones
En raison de son faible coût, l’huile de palme est, depuis quelques années, très utilisée dans l’alimentation: elle est présente dans 1 produit alimentaire empaqueté sur deux vendus en Europe (chips, biscuits, crème glacée, etc.). Or, la plantation de palmiers est à l’origine de déforestation, notamment en Indonésie. Dans ce pays, 3 millions d’hectares de forêt tropicale ont été détruits à cet effet entre 1990 et 2005 et le gouvernement prévoit un plan d’expansion des plantations de palmiers à huile de 14 millions d’hectares. La conversion des forêts en palmiers à huile a montré une perte de 80 à 100% des espèces de mammifères (dont l’orang-outan), reptiles et d’oiseaux dans ces zones  Les animaux se nourrissent d’aliments (céréales, petits animaux, etc.) contenant différents polluants. Au fil du temps, ces derniers s’accumulent dans l’organisme de l’animal et en particulier dans les graisses (phénomène de bioaccumulation). Ainsi, une étude de 2010 a révélé la présence de nombreux pesticides et de PCB dans du saumon et du steak haché achetés dans des supermarchés de la région parisienne
Les animaux se nourrissent d’aliments (céréales, petits animaux, etc.) contenant différents polluants. Au fil du temps, ces derniers s’accumulent dans l’organisme de l’animal et en particulier dans les graisses (phénomène de bioaccumulation). Ainsi, une étude de 2010 a révélé la présence de nombreux pesticides et de PCB dans du saumon et du steak haché achetés dans des supermarchés de la région parisienne  Tout comme les fruits et légumes, le riz peut contenir différents polluants tels que des pesticides, en particulier s’il est issu d’une agriculture intensive classique (non « bio »). Ainsi, une étude de 2010 a révélé la présence d’isoprothiolane et de tricyclazole, 2 pesticides interdits d’usage en Europe, dans du riz acheté dans des supermarchés de la région parisienne
Tout comme les fruits et légumes, le riz peut contenir différents polluants tels que des pesticides, en particulier s’il est issu d’une agriculture intensive classique (non « bio »). Ainsi, une étude de 2010 a révélé la présence d’isoprothiolane et de tricyclazole, 2 pesticides interdits d’usage en Europe, dans du riz acheté dans des supermarchés de la région parisienne  L’eau du robinet est globalement de bonne qualité en France et les normes en vigueur sont généralement respectées
L’eau du robinet est globalement de bonne qualité en France et les normes en vigueur sont généralement respectées  Les fruits et légumes issus de l’agriculture intensive « classique » (c’est à dire non « bio ») contiennent des mélanges à faibles doses de substances chimiques classées, par les instances officielles, cancérogènes certaines, probables ou possibles ou soupçonnées d’être perturbatrices du système endocrinien. C’est ce qu’illustre notamment une étude de 2010 qui a révélé la présence de nombreux pesticides dans des produits achetés dans des supermarchés de la région parisienne
Les fruits et légumes issus de l’agriculture intensive « classique » (c’est à dire non « bio ») contiennent des mélanges à faibles doses de substances chimiques classées, par les instances officielles, cancérogènes certaines, probables ou possibles ou soupçonnées d’être perturbatrices du système endocrinien. C’est ce qu’illustre notamment une étude de 2010 qui a révélé la présence de nombreux pesticides dans des produits achetés dans des supermarchés de la région parisienne  Le lave-vaisselle est généralement moins consommateur en eau (12 L) que le lavage à la main qui dépend beaucoup du manipulateur (10 à 50 L)
Le lave-vaisselle est généralement moins consommateur en eau (12 L) que le lavage à la main qui dépend beaucoup du manipulateur (10 à 50 L)  Le liquide vaisselle est un détergent composé d’agents nettoyants appelés tensioactifs, mais aussi de colorants, conservateurs et parfums de synthèse. Bien que les tensioactifs ont l’obligation d’être biodégradables à 90%
Le liquide vaisselle est un détergent composé d’agents nettoyants appelés tensioactifs, mais aussi de colorants, conservateurs et parfums de synthèse. Bien que les tensioactifs ont l’obligation d’être biodégradables à 90%  Les composés perfluorés (PFC), tels que le téflon, ont la propriété de repousser l’eau, les matières grasses et la poussière. Ils sont ainsi utilisés comme antiadhésif dans de nombreuses poêles et casseroles. Les PFC sont persistants et s’accumulent dans les êtres vivants: certaines études ont révélé la présence de certains PFC dans les cours d’eau et les poissons (dans le foie notamment) ainsi que dans le sang humain
Les composés perfluorés (PFC), tels que le téflon, ont la propriété de repousser l’eau, les matières grasses et la poussière. Ils sont ainsi utilisés comme antiadhésif dans de nombreuses poêles et casseroles. Les PFC sont persistants et s’accumulent dans les êtres vivants: certaines études ont révélé la présence de certains PFC dans les cours d’eau et les poissons (dans le foie notamment) ainsi que dans le sang humain  3,8 millions de tonnes de bisphénol A (BPA) ont été produits en 2006
3,8 millions de tonnes de bisphénol A (BPA) ont été produits en 2006  Ces bouteilles contiennent notamment des phtalates, produits chimiques utilisés en tant que plastifiants et qui font partie de la famille des
Ces bouteilles contiennent notamment des phtalates, produits chimiques utilisés en tant que plastifiants et qui font partie de la famille des
Un commentaire
Vivien Lecomte
test commentaire