
Résidus de médicaments dans l’environnement : quels risques pour les écosystèmes ?
Antibiotiques, antidépresseurs, anti-inflammatoires… Les résidus des médicaments que nous consommons se retrouvent aujourd’hui jusque dans les rivières, les sols et les organismes qui y vivent. A mesure que les études se multiplient, l’ampleur de cette contamination de l’environnement et les risques qu’elle fait peser sur les écosystèmes se précisent. Alors, c’est grave, Docteur ?
1. L’état de la contamination de l’environnement par les résidus de médicaments
1.1 Des médicaments dans (presque) toutes les eaux du globe
Les activités humaines rejettent chaque jour une grande diversité de substances chimiques dans l’environnement. Grâce aux progrès récents des méthodes d’analyses (voir encadré plus bas) et aux nombreuses études qui en découlent, la contamination généralisée des milieux par les pesticides, les retardateurs de flamme, les substances per- et polyfluoroalkylées (PFAS) et d’autres molécules d’origine anthropique est désormais bien documentée. Les médicaments, dont le marché mondial en croissance constante a atteint environ 1 600 milliards de dollars en 2023 (leem 2024), ne font pas exception.
La pollution par les résidus de médicaments est une problématique reconnue à l’échelle mondiale depuis le début des années 2000. Une étude portant sur 258 rivières réparties dans 104 pays illustre l’ampleur de cette contamination (Wilkinson et al. 2022). Sur les 137 zones géographiques étudiées, seules trois ne présentaient aucune trace détectable des substances actives pharmaceutiques recherchées. Et encore, cette étude ne portait que sur 61 substances actives, alors que plus de 3 500 sont actuellement commercialisées dans le monde.
Substance active : de quoi parle-t-on ? (d’après le Ministère de la santé)
Une substance active, également appelé principe actif, est la molécule présente dans le médicament qui lui confère ses propriétés thérapeutiques, diagnostiques ou préventives. Dans un médicament, la substance active est généralement associée à des substances inactives pharmacologiquement (excipients) permettant d’assurer sa mise en forme pharmaceutique, sa stabilité ou sa diffusion dans l’organisme.
Les rivières les moins contaminées se situent principalement dans des régions peu peuplées, comme l’Islande ou la Norvège, ou dans des pays à faible revenu où la consommation de médicaments demeure limitée, tels que la Sierra Leone ou le Zimbabwe. À l’inverse, les niveaux de contamination les plus élevés sont observés dans des pays à revenu intermédiaire disposant d’infrastructures insuffisantes de traitement des eaux usées et accueillant parfois de nombreuses usines pharmaceutiques, comme le Pakistan, la Bolivie ou l’Inde.
Chez nous aussi, les médicaments sont présents dans les eaux. Les concentrations mesurées dans les trois bassins versants français inclus dans l’étude se situent légèrement en dessous de la médiane mondiale. En Espagne, le Rio Manzanares (Photo 1) — qui traverse Madrid et dont le débit est fortement influencé par le climat aride et par un modèle agricole reposant sur l’irrigation — est le cours d’eau européen le plus contaminé. Il figure parmi les 10 % des rivières les plus polluées au monde, avec un cumul dépassant 15 microgrammes de substances actives pharmaceutiques par litre d’eau (µg/L).

Les eaux marines sont elles aussi largement contaminées. En France, une étude prospective menée par l’Ifremer sur 26 points de suivi le long du littoral métropolitain a révélé la présence d’une ou plusieurs substances actives pharmaceutiques dans l’ensemble des sites étudiés (Amouroux et al. 2025). A l’échelle mondiale, une étude portant sur plus de 2 000 échantillons d’eau marine montre que les résidus de médicaments sont largement présents dans les estuaires et les eaux côtières, et que leur concentration diminue à mesure que l’on s’éloigne du littoral (Kalinski et al. 2026).
Dans une moindre mesure, les eaux souterraines peuvent également être contaminées. Une étude menée à l’échelle européenne — couvrant 12 États et ciblant 300 substances — a ainsi mis en évidence des traces de paracétamol dans près d’un quart des sites étudiés (OECD 2019).
Les progrès de la chimie analytique (Agence de l’eau Adour-Garonne et OFB 2022)
D’importants progrès ont été réalisés au cours des vingt dernières années dans la caractérisation de la contamination chimique des milieux. Grâce à l’amélioration des techniques analytiques, en particulier en spectrométrie de masse, les chimistes sont désormais capables d’identifier plusieurs milliers de molécules. La sensibilité des méthodes s’est également considérablement accrue : alors qu’au début des années 2000, seules les substances présentes à des concentrations supérieures au microgramme par litre pouvaient être détectées (niveau des « traces »), les méthodes actuelles permettent d’atteindre le nanogramme par litre (ultra‑traces), voire le picogramme par litre lorsque cela est nécessaire (ultra‑ultra‑traces). Ces avancées rendent visibles des molécules auparavant « invisibles », ce qui constitue un progrès majeur pour la compréhension de la contamination. Elles peuvent toutefois introduire un biais d’interprétation : plus on recherche de substances avec des méthodes plus sensibles, plus on en détecte.
1.2 Une véritable pharmacie dans les rivières
Les études consacrées à la contamination des rivières révèlent la présence simultanée de nombreuses substances actives issues de médicaments appartenant à des classes thérapeutiques variées. Cette diversité témoigne de l’empreinte chimique laissée par nos pratiques de santé sur l’environnement.
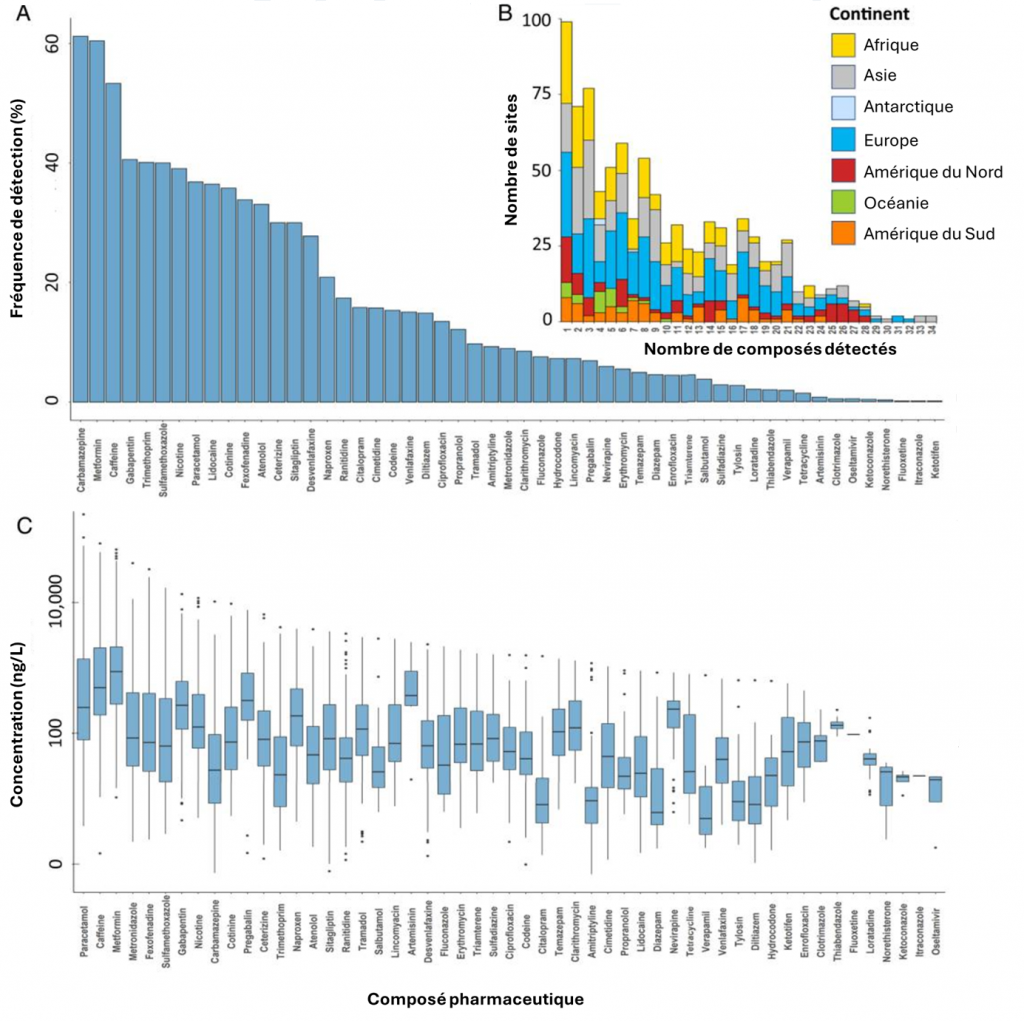
A l’échelle mondiale, les substances les plus souvent détectées dans les cours d’eau – présentes dans environ 60 % des sites étudiés par Wilkinson et al. (2022) – sont la carbamazépine et la metformine (voir Figure 1(A)). La carbamazépine est un antiépileptique également utilisé pour traiter certaines douleurs liées au système nerveux. La metformine, quant à elle, est un médicament de référence dans la prise en charge du diabète de type 2, souvent associé à l’obésité. D’autres substances sont également très répandues, notamment la gabapentine (antiépileptique) ainsi que les antibiotiques triméthoprime et sulfaméthoxazole, retrouvés dans environ 40 % des sites d’échantillonnage.
En termes de concentration, la metformine et le paracétamol — l’antalgique le plus consommé au monde — sont les substances les plus abondantes dans les eaux. Le paracétamol détient même la concentration maximale mesurée à l’échelle mondiale : 227 µg/L, relevés dans la rivière Rio Seke, à La Paz (Bolivie).
Quelques repères sur les concentrations
-1 microgramme (µg) est 1 000 000 fois plus léger qu’1 gramme (g)
-1 nanogramme (ng) est 1 000 fois plus léger qu’1 microgramme (µg)
-1 morceau de sucre dans un bassin olympique = 1 µg/L
-1 grain de sel dans un bassin olympique = 1 ng/L
En France, la surveillance menée par les agences de l’eau Rhône-Méditerranée Corse (période 2021-2023) et Seine-Normandie (période 2020-2023) nous éclaire sur les substances actives les plus présentes dans nos rivières. La metformine, toujours elle, arrive en tête dans ces deux bassins : elle est détectée dans plus de 80 % des échantillons. En plus de la metformine, plusieurs substances figurant dans le TOP 20 des molécules les plus vendus en France (chiffres 2024) sont détectées dans plus d’un échantillon sur quatre. Il s’agit de l’oxazépam (anxiolytique), du tramadol (antalgique), du paracétamol et du diclofénac (anti-inflammatoire). Sur le bassin Seine-Normandie, les concentrations moyennes les plus élevées concernent la metformine (0,2 µg/L) et le paracétamol (0,05 µg/L).
D’autres molécules fréquemment détectées sur les deux bassins, comme l’irbésartan (traitement de l’hypertension), le sotalol (traitement des maladies cardiovasculaires) et le sulfaméthoxazole (antibiotique), ne figurent pas parmi les médicaments les plus vendus en France. Cela montre que le niveau de consommation n’est pas le seul facteur explicatif : les propriétés physico-chimiques des molécules jouent également un rôle déterminant dans leur persistance et leur concentration dans l’environnement.
Ce « palmarès » des substances les plus présentes dans les rivières doit toutefois être interprété avec prudence, car on ne trouve que ce que l’on cherche ! Ainsi, l’amoxicilline, pourtant premier antibiotique prescrit en France, n’a pas été analysée dans ces études, pas plus que les substances à usage exclusivement vétérinaire.
10 tonnes de paracétamol dans la Seine !
Les concentrations en résidus de médicaments mesurées dans les rivières françaises sont – heureusement – faibles. Mais si l’on raisonne non plus en concentration, mais en flux, c’est-à-dire en masse de substance active transportée par une rivière en tenant compte de son débit, les ordres de grandeurs changent radicalement. On estime ainsi qu’environ 10 tonnes de paracétamol transitent chaque année dans la Seine en aval de Paris, au niveau de Poissy (INRAE et Graie 2022). Cela représente environ 1 % de la quantité vendue sur le bassin versant. Pour le diclofénac, une molécule qui se dégrade moins facilement que le paracétamol, le flux annuel est d’environ 1 tonne, ce qui correspond à 13 % de la quantité consommée sur le bassin.
1.4 Des données encore limitées sur la contamination des sols
Contrairement aux milieux aquatiques, la contamination des sols par les résidus de médicaments reste peu documentée. Les travaux existants portent principalement sur des zones exposées à l’épandage de boues ou d’effluents de stations d’épuration, ou encore à l’application d’engrais d’origine animale.
A titre d’illustration, on peut citer une étude menée par des chercheurs espagnols, portant sur l’impact de l’irrigation de sols avec des eaux usées traitées (Biel-Maeso et al. 2018). Leurs analyses montrent que la couche superficielle du sol irrigué peut contenir jusqu’à 15 µg de substances actives pharmaceutiques par kilogramme de sol, avec une prédominance d’analgésiques et d’anti-inflammatoires. Des substances actives ont également été détectées jusqu’à 1,50 m de profondeur, indiquant que ces substances peuvent être entraînées par lessivage lors d’épisodes de fortes pluies.
1.5 Des résidus de médicaments jusque dans les plantes et les animaux
Une fois dans les sols, certaines substances actives peuvent être absorbées par les plantes qui y poussent (Gworek et al. 2021). Une étude menée sur un sol contaminé par de la carbamazépine a ainsi montré qu’environ un tiers de la masse initiale de la substance présente dans le sol s’accumulait dans les parties aériennes (feuilles, tiges, graines…) d’une plante fourragère cultivée sur ce sol (Winker et al. 2010).
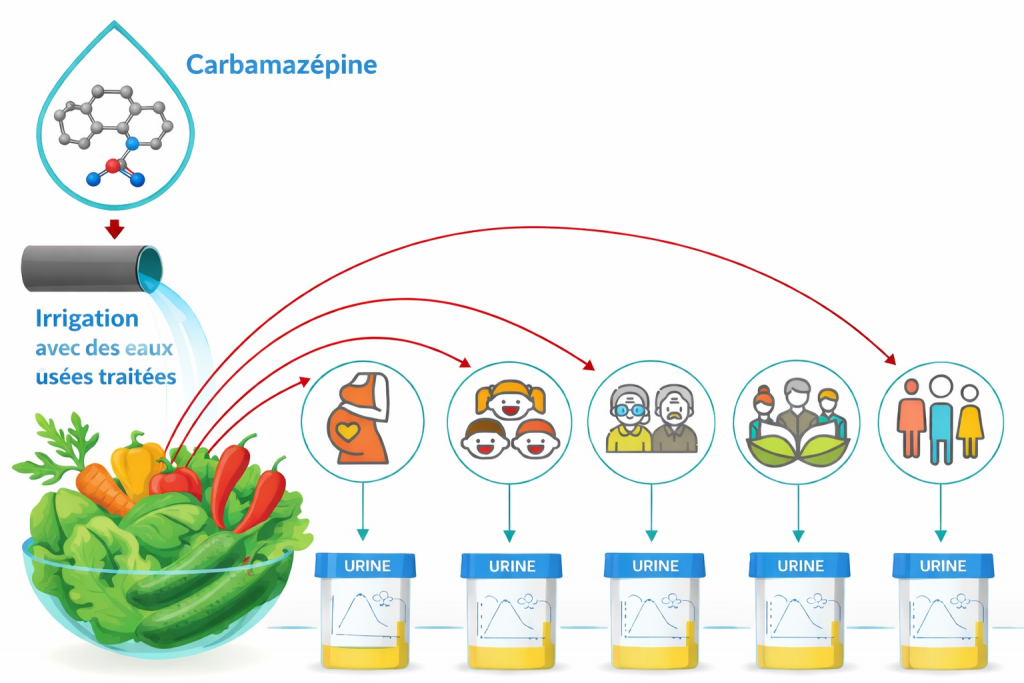
En Israël, où la réutilisation des eaux usées traitées pour l’irrigation est largement répandue, des chercheurs de l’Université de Jérusalem ont détecté des traces de carbamazépine dans des concombres, carottes, laitues et piments (Figure 2). Ils ont également retrouvé cette substance dans les urines de personnes ayant consommé ces légumes, en particulier chez les individus se déclarant végétariens ou suivant les recommandations nutritionnelles en matière de consommation de fruits et légumes (Paltiel et al. 2016 ; Schapira et al. 2020).
Les organismes vivant dans les milieux aquatiques sont eux aussi largement contaminés par le cocktail de médicaments présents dans les eaux. Une vaste étude bibliographique internationale portant sur les invertébrés (crustacés, mollusques, etc.) et les poissons d’eaux douces et marines a recensé 77 substances actives pharmaceutiques dont la présence est détectée dans au moins 10 % des organismes analysés (Lecomte et al. 2023a).
Parmi elles figurent des substances utilisées en neurologie et en psychiatrie (carbamazépine, citalopram, etc.), en cardiologie (clonidine, hydrochlorothiazide, etc.), mais aussi des antibiotiques(clarithromycine, ciprofloxacine, etc.), des antiviraux— comme l’éfavirenz, utilisé dans le traitement du VIH —, des antiparasitaires tels que le lévamisole (vermifuge), ainsi que des analgésiques et anti‑inflammatoires (kétoprofène, diclofénac, etc.).
Plus surprenant encore, l’étude révèle que les organismes aquatiques sont également contaminés par des drogues illicites. D’après les données disponibles, près de deux tiers des invertébrés présentent des traces de cocaïne, et 13 % d’entre eux de l’amphétamine.
1.6 Quand les médicaments se transforment
Ces observations ne racontent toutefois qu’une partie de l’histoire : dans l’environnement comme dans les organismes, les substances actives ne restent pas toujours sous leur forme initiale.
Lorsque nous (ou d’autres animaux) consommons un médicament, notre organisme – qui reconnaît la substance active comme une substance étrangère – met en œuvre différents mécanismes pour l’éliminer. La substance active est alors excrétée, principalement via les urines, soit sous forme inchangée (on parle de « molécule mère »), soit après avoir subi des transformations chimiques, notamment dans le foie. Ces transformations produisent de nouvelles molécules appelées métabolites.
De telles transformations peuvent également avoir lieu dans le réseau d’assainissement (les égouts), dans les stations d’épuration, dans les milieux naturels ainsi qu’au sein des organismes qui y vivent.
C’est pourquoi, outre les substances actives présentes dans la formulation du médicament, de nombreux travaux scientifiques mettent en évidence la présence de métabolites de médicaments dans l’environnement. Par exemple, dans le cadre d’une étude portant sur la Vienne et ses affluents, des chercheurs de l’institut de chimie de Poitiers ont détecté, chez des corbicules (mollusques bivalves d’eau douce), non seulement de la carbamazépine et du diclofénac, mais aussi cinq de leurs métabolites (Zind et al. 2021).
Composé parent ou métabolite ?
Il n’est pas toujours simple d’identifier l’origine d’un résidu de médicament détecté dans l’environnement. L’oxazépam, par exemple, est à la fois la substance active d’un médicament spécifique et un métabolite de plusieurs anxiolytiques (comme le diazépam ou le témazépam).
2. Comment les résidus de médicaments contaminent l’environnement
Les résidus de médicaments se dispersent dans l’environnement par un réseau complexe de voies de contamination, illustré sur la Figure 3. Nous distinguons trois principales sources, que seront détaillées dans ce chapitre : (i) les rejets liés à l’usage des médicaments chez l’humain, (ii) les rejets issus des usages vétérinaires et (iii) les rejets directs des industries pharmaceutiques.
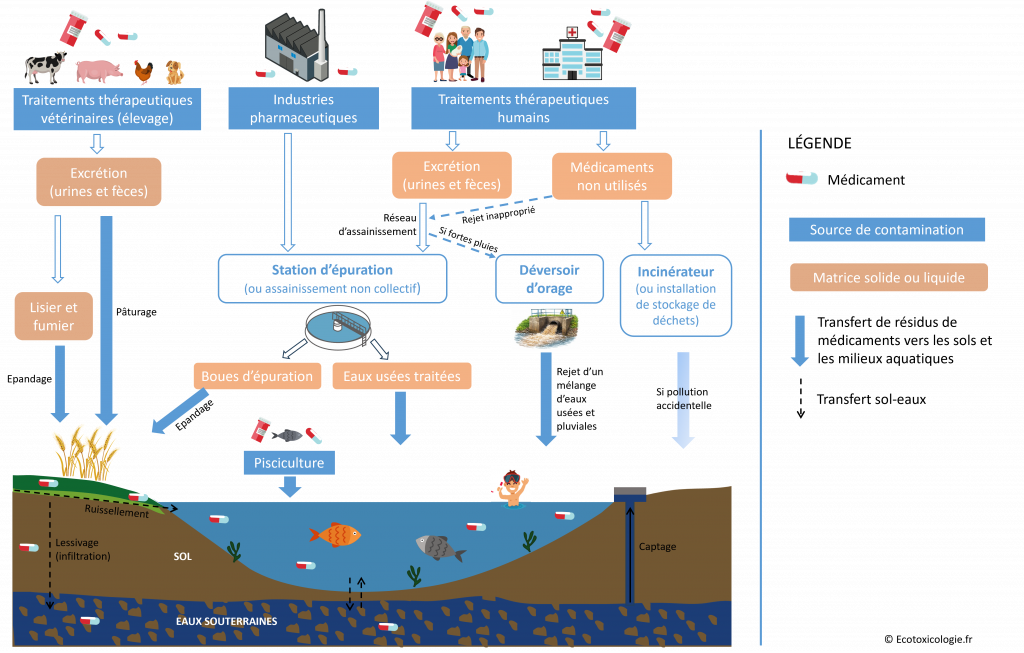
2.1 Les rejets liés à l’usage des médicaments chez l’humain
L’excrétion via les urines ou les selles constitue la principale source de rejet de résidus de médicaments à usage humain dans l’environnement, loin devant l’élimination inappropriée des médicaments non utilisés et les effluents des industries pharmaceutiques. En effet, contrairement à une idée reçue, le rejet de restes de médicaments dans l’évier, les toilettes ou la poubelle d’ordures ménagères ne contribue que de façon mineure à la contamination environnementale (OECD 2019).
2.1.1 De l’administration du médicament à son excrétion par l’organisme
Mais pour comprendre pourquoi l’excrétion constitue la principale source de contamination, intéressons-nous au parcours d’un médicament, de son ingestion par l’organisme jusqu’à son éventuel rejet dans l’environnement.
Lorsque nous ingérons un médicament (comprimé, gélule, sirop…), la substance active responsable de l’effet thérapeutique passe dans le sang via le système digestif. Elle est ensuite transportée vers différents organes, où elle interagit avec une cible biologique (enzyme, récepteur, micro-organisme, etc.). C’est cette interaction qui produit l’effet thérapeutique recherché.
Une partie des substances passe par le foie, qui agit comme une véritable « usine chimique » capable de transformer les molécules. Cette transformation, à l’origine de la production des métabolites évoqués précédemment, peut activer ou inactiver la substance, ou encore faciliter son élimination par l’organisme.
L’élimination de la substance active ou de ses métabolites se fait principalement au niveau des reins, qui filtrent le sang et dirigent ces molécules vers l’urine (Figure 4). Certaines substances sont également excrétées dans la bile (produite par le foie) puis éliminées dans les selles.
Au final, on estime que 30 à 90 % des doses de substances actives ingérées sont excrétées, sous leur forme initiale ou sous forme de métabolites actifs (BIO Intelligence Service 2013), ce qui représente des quantités très importantes à l’échelle d’une population. Ce taux d’excrétion dépend des propriétés de la substance active, de son mode et de sa dose d’administration, ainsi que des caractéristiques du patient.
2.1.2 De son rejet dans les eaux usées à son arrivée en station d’épuration
Une fois excrétés, les résidus de médicaments rejoignent les eaux usées via les toilettes. Ces eaux sont généralement collectées par un réseau d’assainissement public, puis acheminées vers une station d’épuration (Figure 3).
Deux exceptions sont toutefois à noter. Premièrement, lorsque le réseau d’assainissement collecte à la fois les eaux usées et les eaux pluviales, il peut déborder en cas de fortes pluies. Une partie des eaux usées, ainsi que les résidus de médicaments qu’elles contiennent, est alors rejetée directement dans le milieu naturel, au niveau d’un ouvrage appelé déversoir d’orage. Deuxièmement, une partie de la population n’est pas raccordée au réseau d’assainissement public et dispose de son propre dispositif de traitement, communément appelé fosse septique. Cet « assainissement non collectif » (ANC) concerne environ 15 % de la population française (Ofb.gouv.fr, 2023).
Contrairement à une (seconde) idée reçue, les hôpitaux ne sont pas les principaux contributeurs aux rejets de résidus de médicaments dans les eaux usées. Sur le territoire du bassin d’Arcachon, par exemple, le flux de paracétamol apporté par le réseau urbain (> 1kg/jour) est nettement plus élevé que celui provenant de l’hôpital local (environ 100 g/jour) (Figure 5 – projet REMPAR). Plus globalement, les études montrent que les effluents des établissements de soin, bien que plus concentrés que les eaux usées urbaines, ne représentent en moyenne que 15 à 20 % de la charge totale en résidus de médicaments arrivant à la station d’épuration d’une l’agglomération (Dagot 2018). Rien d’étonnant, finalement, lorsque l’on sait que la majorité des médicaments est consommée en dehors des hôpitaux.
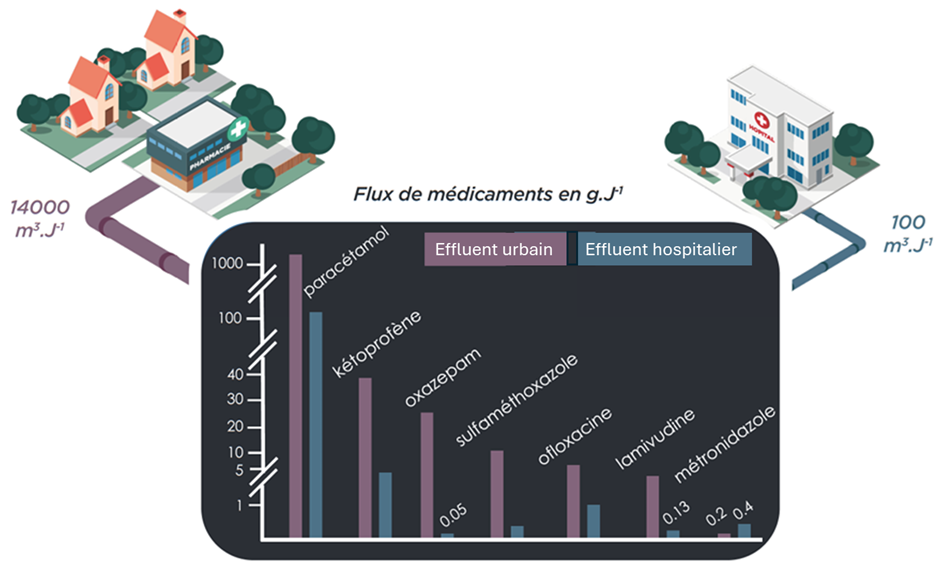
Il existe toutefois quelques exceptions pour lesquelles l’apport hospitalier est majoritaire, comme les antibiotiques réservés à des affections sévères (par exemple la vancomycine), certains traitements anticancéreux ou encore des agents de contraste utilisés en imagerie médicale (gadolinium) (Lecomte et al. 2018).
Plus de 1 mg de paracétamol par litre d’eau usée !
Les concentrations en résidus de médicaments dans les eaux usées sont faibles, mais très variables selon les substances : inférieures à 0,1 µg/L pour les hormones (estrone, 17β-estradiol, oestriol) ; comprises entre 0,1 et 10 µg/L pour un grand nombre de substances ; et supérieures à 10 µg/L, voire à 100 µg/L pour des substances comme l’aspirine et le paracétamol (Dagot 2018 ; Thiebault 2024). Pour ce dernier, des concentrations supérieures à 1 mg/L ont même été mesurées dans des effluents hospitaliers (SIPIBEL 2016).
2.1.3 Une partie des résidus de médicaments passe entre les mailles du traitement
Les stations d’épuration actuelles ont été conçues pour éliminer la matière organique, d’abord carbonée, puis azotée et phosphorée (Dagot 2018). Elles n’ont pas été pensées pour traiter des substances chimiques présentes à l’état de trace et aux propriétés très diverses, comme les résidus de médicaments.
Les phénomènes de « sorption » (fixation aux particules solides) et de « biotransformation » (transformation par les microorganismes) qui se produisent au sein de ces stations peuvent néanmoins permettre d’atteindre un rendement d’élimination global d’environ 50 % du flux de résidus de médicaments entrant (Dagot 2018).

Ce rendement d’élimination, également appelé taux d’abattement, est très variable selon le type de traitement mis en œuvre, et surtout, selon les propriétés intrinsèques de la substance à traiter.
Le tableau 1 illustre cette variabilité pour des substances actives appartenant à diverses classes thérapeutiques, dans le cas des stations d’épuration « à boues activées » (type de station le plus répandu en France) (Cemagref 2009). Certaines substances comme le paracétamol (dont le taux d’abattement est généralement supérieur à 90 %) ou le bromazépam (anxiolytique) sont très bien éliminées. A l’inverse, d’autres, comme le diclofénac et la carbamazépine, sont plus réfractaires aux traitements.
| Rendement d’élimination élevé (> 70 %) | Rendement d’élimination moyen (entre 30 et 70 %) | Rendement d’élimination faible (< 30 %) | |
| Antalgiques et anti-inflammatoires | Paracétamol Ibuprofène Kétoprofène | Diclofénac | |
| Antibiotiques | Oxytétracycline* | Roxithromycine Sulfaméthoxazole | |
| Cardiologie et angiologie | Nadolol Acébutolol | Aténolol Métoprolol | Sotalol Propranolol |
| Hormones et endocrinologie | Œstrone Œstradiol Œstriol | ||
| Neurologie et psychiatrie | Imipramine Bromazépam | Amitriptyline Fluoxétine | Carbamazépine Diazépam |
| Pneumologie | Clenbutérol | Salbutamol Terbutaline |
Une partie des résidus de médicaments entrant dans les stations d’épuration est donc rejetée dans le milieu aquatique (rivière, fleuve ou lac) via les eaux usées traitées. Les concentrations de résidus de médicaments dans ces rejets peuvent atteindre le ng/L ou le µg/L selon les substances (Lecomte et al. 2023b).
Les résultats des analyses réalisées à la station d’épuration de Bellecombe, en Haute-Savoie, dans le cadre du programme SIPIBEL, ont révélé la présence de substances réfractaires au traitement, comme le diclofénac et la carbamazépine, dans plus de 70 % des échantillons en sortie de station. Ils ont également mis en évidence la présence de substances pourtant bien éliminées, mais dont la concentration en entrée de station était très élevée, comme le paracétamol et l’ibuprofène (Lecomte et al. 2018).

Enfin, une (petite) partie des résidus de médicaments est transférée dans les boues d’épuration (photo 3), principal déchet du traitement des eaux usées. Il s’agit de substances peu biodégradables, dont les propriétés favorisent leur fixation sur la matière organique et les particules solides, entraînant leur accumulation dans les boues plutôt que leur élimination complète.
Dans la station d’épuration de Bellecombe citée précédemment, les concentrations les plus élevées ont été mesurées pour la ciprofloxacine (détectée dans 100 % des échantillons analysés, à des concentrations allant de 28 µg à 5,9 mg par kg de matière sèche) et la tétracycline (détectée dans 80 % des échantillons, de 19 µg à 8 mg par kg de matière sèche), deux antibiotiques (Etienne 2024).
En France, environ trois quarts des boues de stations d’épuration sont épandues sur les terres agricoles en tant qu’engrais (INRA et al. 2014), contribuant ainsi à la contamination des sols par les résidus de médicaments.
Quelle est la surveillance réglementaire des résidus de médicaments dans l’environnement ?
Ce n’est que récemment que l’Europe s’est saisie de la question de surveillance des résidus de médicaments dans les eaux. Dans le cadre de la directive cadre sur l’eau (DCE), la France, via l’arrêté du 26 avril 2022, a établi une liste de « substances pertinentes à surveiller” (SPAS) dans les eaux de surface et souterraines comprenant, entre autres : un antiépileptique (carbamazépine) et son métabolite, quatre anti-inflammatoires/analgésiques (diclofénac, ibuprofène, kétoprofène, paracétamol), deux métabolites de l’ibuprofène, trois antibiotiques (sulfaméthoxazole, ofloxacine, ciprofloxacine), deux anxiolytiques (oxazépam, diazépam), un hypolipémiant (acide fénofibrique), un anticancéreux (cyclophosphamide) et un bêta-bloquant (sotalol).
Huit de ces substances peuvent également être suivies de façon optionnelle dans les eaux usées des stations d’épuration urbaines, dans le cadre des campagnes RSDE (Recherche de Substances Dangereuses dans l’Environnement).
En revanche, il n’existe à ce jour aucune valeur limite réglementaire concernant les rejets de résidus de médicaments par les stations d’épuration, même si cela devrait évoluer dans les prochaines années avec la révision de la directive eaux résiduaires urbaines (DERU). De même, aucune limite de concentration n’est actuellement fixée pour les résidus de médicaments dans les boues d’épuration ou dans les sols.
2.2 Les rejets issus des usages vétérinaires
2.2.1 Les usages des médicaments vétérinaires
Mais les médicaments ne sont pas uniquement utilisés chez l’humain : une part importante d’entre eux est également destinée aux animaux.
Les médicaments vétérinaires servent essentiellement à traiter (antibiotiques, anti-inflammatoires, etc.) et à prévenir (vaccins, antiparasitaires, etc.) les maladies des animaux d’élevage. Certains sont également utilisés pour optimiser la reproduction et la gestion des troupeaux (hormones de reproduction, traitements liés à la gestation ou à la lactation, etc.). Enfin, une fraction plus réduite est destinée à la médecine des animaux de compagnie.
Pour mieux appréhender la contribution potentielle des usages vétérinaires à la contamination de l’environnement, il est utile d’avoir en tête quelques ordres de grandeur. Aux États-Unis, d’après la FDA (Food and Drug Administration), environ 6 000 tonnes d’antibiotiques à usage vétérinaire ont été vendues en 2020, soit environ deux fois plus que pour les usages humains (3 300 tonnes).
En France, en revanche, grâce à la réglementation et aux plans nationaux Ecoantibio — qui ont permis de réduire de 79 % l’utilisation des antibiotiques vétérinaires entre 1999 et 2022 —, la médecine vétérinaire consomme aujourd’hui nettement moins d’antibiotiques (environ 276 tonnes en 2022, d’après l’ANSES) que la médecine humaine (plus de 750 tonnes par an, d’après l’ANSM), même si ces quantités restent considérables.
Il est également possible de comparer le nombre de substances actives autorisées en France : environ 2 800 pour la médecine humaine (ANSM 2016) et près de 900 pour la médecine vétérinaire (ANSES 2024). Certaines substances sont utilisées à la fois chez l’humain et chez l’animal, notamment des antibiotiques comme le sulfaméthoxazole.
2.2.2 Des déjections animales directement rejetées dans l’environnement
Comme pour les humains, la principale voie de dissémination environnementale des résidus de médicaments vétérinaires est l’excrétion. Mais, à la différence des humains — dont les déjections sont traitées en station d’épuration —, il n’existe pour les animaux d’élevage aucun « filtre » équivalent capable d’éliminer une partie des substances excrétées.
En effet, les déjections animales, ainsi que les résidus de médicaments qu’elles peuvent contenir, rejoignent souvent directement le milieu : soit lors du pâturage, soit lors de l’épandage de fumier (mélange de déjections animales et de litière) ou de lisier (mélange de déjections animales et d’eau) sur les cultures (Photo 4).
Pour donner un ordre de grandeur, environ 300 millions de tonnes de matières fertilisantes organiques d’origine animale sont épandues chaque année en France, contre environ 1,1 million de tonnes de boues d’épuration (ADEME Pays-de-la-Loire 2018). Cela illustre l’importance potentielle de cette voie de transfert de contaminants vers l’environnement.

Les niveaux de contamination des fumiers et lisiers sont encore relativement mal connus et dépendent fortement des pratiques d’élevage, ainsi que d’autres paramètres, comme leur durée de stockage.
En Espagne, une étude menée sur des matières fertilisantes issues d’élevages intensifs a notamment détecté la présence d’oxytétracycline(un antibiotique) dans 37 % des échantillons de fumier de volaille et dans 20 % des échantillons de lisier de porc, avec une concentration moyenne de 275 µg/kg (Carballo et al. 2016).
En France, dans le cadre du programme SIPIBEL, une étude a comparé des lisiers et fumiers issus d’élevages de vaches laitières avec des boues de station d’épuration, à partir de l’analyse de 28 substances pharmaceutiques (Etienne et al. 2024). Les résultats montrent que les fumiers et lisiers sont globalement moins contaminés que les boues, avec moins de substances détectées et des concentrations plus faibles. Une dizaine de substances ont néanmoins été retrouvées, appartenant aux familles des antibiotiques, des antiparasitaires et des anti-inflammatoires. Dans le lisier, les concentrations les plus élevées ont été mesurées pour le 3-amino-5-méthylisoxazole, métabolite de l’antibiotique sulfaméthoxazole (jusqu’à 14,4 µg/kg) ainsi que pour la tétracycline (jusqu’à 1,4 µg/kg) et son métabolite épi-tétracycine (jusqu’à 1,7 µg/kg).
Des concentrations nettement plus faibles que celles relevées dans l’étude espagnole — pourtant déjà situées dans la fourchette basse de la littérature internationale. Ces résultats illustrent l’ampleur de la variabilité des niveaux de contamination de ces matières fertilisantes d’origine animale.
Enfin, les carcasses d’animaux d’élevage ayant consommé des médicaments peuvent également constituer une source de contamination environnementale, comme en témoigne l’histoire tristement célèbre des vautours intoxiqués au diclofénac, sur laquelle nous reviendrons par la suite.
2.3 Les rejets des usines pharmaceutiques
La production de médicaments est aujourd’hui largement mondialisée. La majorité des médicaments consommés en France sont fabriqués ailleurs en Europe, tandis que les substances actives qui les composent proviennent souvent d’Asie, notamment d’Inde et de Chine (Poterszman et Pouzet 2026). C’est pourquoi, en France, les rejets directs des usines pharmaceutiques constituent une source mineure de contamination environnementale, en comparaison de l’excrétion humaine et animale.
En revanche, dans les régions du monde où se concentre la production de substances actives pharmaceutiques et où les normes de rejet sont peu contraignantes ou insuffisamment appliquées, les effluents industriels peuvent représenter une source de contamination localement très importante . Des concentrations extrêmement élevées — de l’ordre du milligramme par litre — ont été mesurées dans certains effluents et dans les cours d’eau récepteurs, notamment en Inde, en Chine, aux États-Unis, en Corée ou encore en Israël (Larsson 2014).
L’exemple le plus emblématique est sans doute celui d’une station d’épuration située à Patancheru, près d’Hyderabad, en Inde (Photo 5), qui traite les effluents d’environ 90 usines pharmaceutiques. Des concentrations de ciprofloxacine atteignant 32 mg/L y ont été mesurées (Larsson et al. 2007), soit des niveaux supérieurs à ceux observés dans le sang de patients traités avec cet antibiotique !

>> EN RESUME
En France, où les usines pharmaceutiques sont peu nombreuses et où un dispositif de gestion des médicaments non utilisés (éco-organisme Cyclamed) est en place, la présence de résidus de médicaments dans les sols et les eaux dépend principalement de leurs usages thérapeutiques humain et vétérinaire, des quantités consommées, de leur taux d’excrétion et de leur capacité à se dégrader naturellement dans l’environnement ou lors du traitement en station d’épuration (ANSES 2020).
3. Que deviennent les résidus de médicaments une fois dans l’environnement ?
Une fois libérés dans le milieu naturel, les résidus de médicaments n’ont pas terminé leur parcours. Leur devenir dépend à la fois de leurs propriétés intrinsèques (biodégradabilité, affinité pour l’eau ou pour les particules solides, etc.) et des caractéristiques du milieu dans lequel ils se trouvent.
Selon ces paramètres, ils peuvent :
- être transférés d’un compartiment environnemental à un autre ou, au contraire, être fixés ;
- se transformer, être totalement dégradés ou bien persister sous leur forme initiale ;
- s’accumuler dans les organismes vivants.
Ces différents processus — transfert, transformation et bioaccumulation — déterminent la présence et le devenir des résidus de médicaments dans les écosystèmes, ainsi que leurs impacts potentiels sur les organismes vivants.
3.1 Des transferts complexes entre sols et eaux
Les résidus de médicaments peuvent être plus ou moins mobiles dans l’environnement. Prenons deux cas pour l’illustrer :
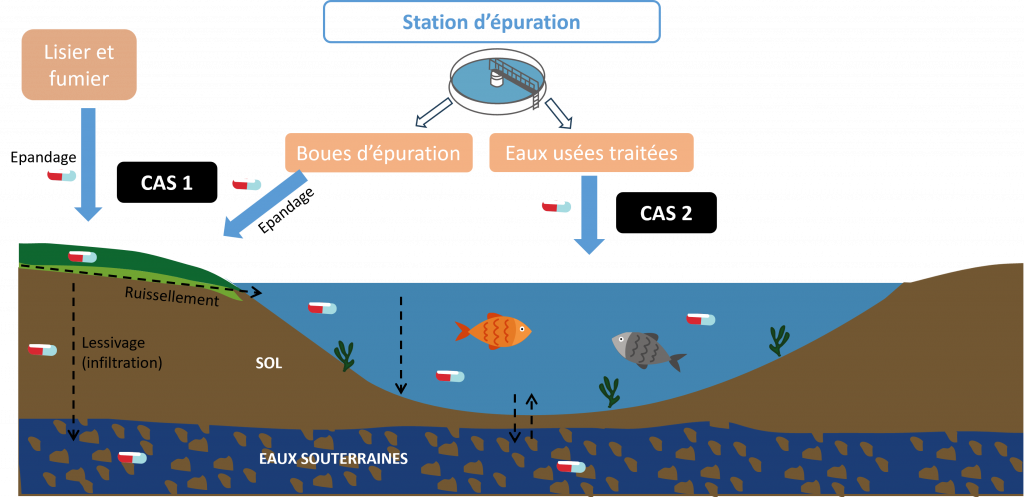
CAS 1 : un résidu de médicament rejoint le sol à la suite d’un épandage de boues, de lisier ou de fumier. Il peut être retenu durablement dans la couche arable (couche supérieure du sol) par « sorption » (fixation) sur les particules solides du sol. Mais, en cas de pluie, il peut aussi être entraîné vers une rivière par ruissellement. Enfin, par infiltration, il peut migrer vers les couches plus profondes du sol, voire jusqu’à une nappe d’eau souterraine.
Les résultats de plusieurs études menées en France sont toutefois plutôt rassurants quant à cette contamination potentielle des nappes phréatiques liée aux pratiques d’épandage (Deschamps et al. 2017 ; Etienne et al. 2024). Dans le cadre du programme de SIPIBEL, par exemple, aucune accumulation significative de résidus de médicaments dans les sols n’a été observée après deux ans d’épandage de lisier et de boues d’épuration à des doses agronomiques. De plus, les flux de résidus de médicaments vers les eaux souterraines représentent globalement une très faible fraction des quantités apportées en surface (Etienne 2024).
CAS 2 : un résidu de médicament rejoint une rivière via les effluents d’une station d’épuration. Il peut rester dans la colonne d’eau, sous forme dissoute ou fixé sur des particules. Il peut également se déposer dans les sédiments (particules solides du fond de la rivière). Dans les deux cas, il peut, sous l’effet du courant, poursuivre son voyage au fil de l’eau, et pourquoi pas un jour, atteindre le milieu marin. Des échanges entre la rivière et la nappe phréatique peuvent aussi conduire à son transfert vers les eaux souterraines.
3.2 Des transformation plus ou moins rapides
Une fois dans le milieu naturel, un résidu de médicament peut subir de nouvelles transformations, cependant moins intenses que celles observées en station d’épuration. Les travaux scientifiques suggèrent que la biodégradation (action des micro-organismes) et la photodégradation (effet de la lumière) sont les deux principaux mécanismes en jeu (Fernandes et al. 2021).
Mais les médicaments ne sont pas tous égaux face à ces phénomènes. Ainsi, dans une rivière, le paracétamol et la fluoxétine sont généralement dégradés relativement rapidement par l’action des communautés microbiennes, avec une demi-vie de l’ordre de quelques jours (Benotti et Brownawell 2009 ; Lin et al. 2010). A l’inverse, la carbamazépine est beaucoup plus persistante, avec une demi-vie allant de plusieurs centaines à plusieurs milliers de jours (Li et al. 2016 ; Posselt et al. 2020)
Bien sûr, comme nous l’avons vu précédemment, ces processus de dégradation ne conduisent pas toujours à une disparition complète de la substance pharmaceutique : ils peuvent aussi produire des métabolites, dont les propriétés (persistance, capacité de bioaccumulation, etc.) et les effets peuvent différer de ceux de le substance initiale.
3.3 Une bioaccumulation variable selon les substances et les espèces
Les résidus de médicaments présents dans les milieux naturels peuvent se « bioaccumuler » dans les organismes vivants. C’est particulièrement le cas des substances dites hydrophobes (« qui n’aiment pas l’eau »), qui ont tendance à s’accumuler dans les tissus graisseux.
Deux études scientifiques récentes illustrent ce phénomène, dont l’ampleur varie fortement selon la substance, l’organisme et le milieu étudiés.
Je vous emmène tout d’abord en Afrique du Sud, dans l’estuaire de Zandvlei situé au Cap (Murgatroyd et al. 2025). Cet estuaire est affecté par une pollution liée à des infrastructures de traitement des eaux usées défaillantes ou vieillissantes, à des quartiers non raccordés aux réseaux d’assainissement, ainsi qu’à des ruissellements agricoles et urbains.
Sans surprise, les sept substances actives recherchées dans l’eau par des chercheurs de l’université locale, ont toutes été détectées, à des concentrations de l’ordre du nanogramme ou du microgramme par litre. Mais ce qui est plus marquant, c’est que certaines substances, notamment la carbamazépine et le sulfaméthoxazole, ont été retrouvées dans des crevettes de sable qui y vivent (Kraussillichirus kraussi) à des concentrations plus de 5 000 fois supérieures.
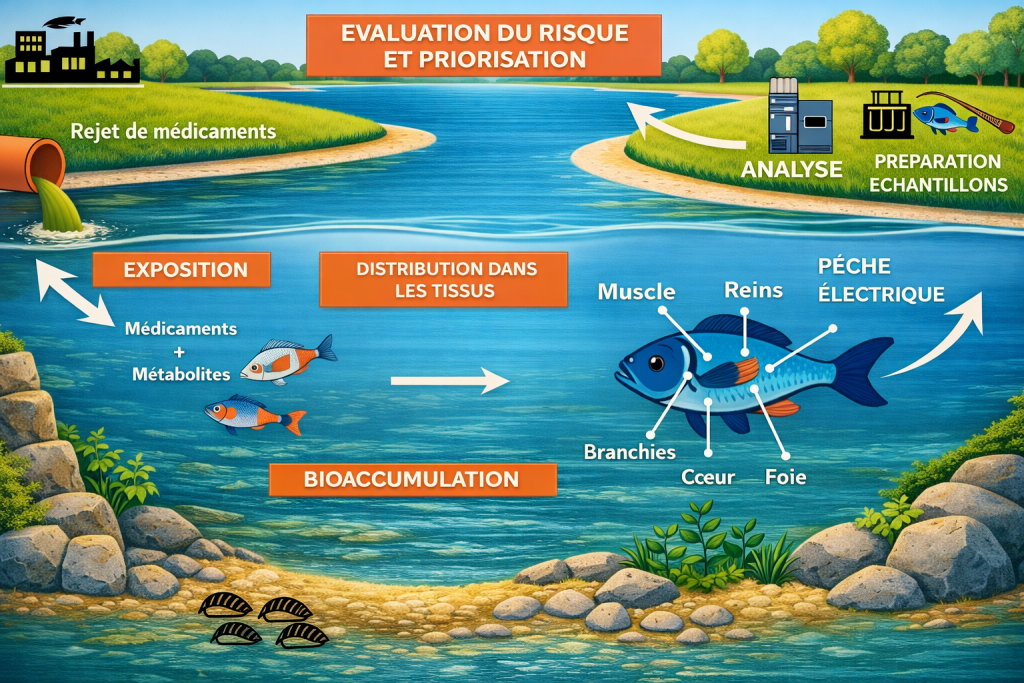
Pour la seconde étude, direction la Croatie, dans la rivière Sava, au niveau d’une zone influencée par les rejets de plusieurs stations d’épuration urbaines et industrielles (Terzic et al. 2024). Dans cette étude, 43 substances (substances actives et métabolites) ont été recherchés dans l’eau ainsi que dans différents tissus de poissons autochtones, échantillonnés par pêche électrique (Figure 6).
Les résultats montrent une contamination généralisée, à la fois dans l’eau et dans les poissons, avec une forte variabilité selon la distance aux points de rejets. Ils indiquent également que certaines substances présentent un fort potentiel de bioaccumulation — comme la sertraline (antidépresseur), la terbinafine (antifongique) ou la loratadine (antihistaminique) — tandis que la majorité se bioaccumule peu ou pas.
Enfin, l’étude met en évidence que les reins et le foie sont les organes où les concentrations sont les plus élevées, suggérant une affinité particulière de ces substances pour ces tissus.
4. Pourquoi les résidus de médicaments représentent-ils un enjeu environnemental majeur ?
ARGUMENT 1 – Les résidus de médicaments sont des « micropolluants »
La première raison pour laquelle les résidus de médicaments constituent un enjeu environnemental majeur tient à leur nature même.
Les substances actives entrant dans la formulation des médicaments sont conçues pour interagir avec les organismes vivants à très faibles doses. Ainsi, même des concentrations minimes dans l’environnement peuvent provoquer des effets involontaires sur les écosystèmes (OECD 2019). A ce titre, tout comme les pesticides, les PFAS ou les PCB, les résidus de médicaments peuvent être qualifiés de « micropolluants », c’est-à-dire des substances susceptibles d’avoir des effets biologiques à des concentrations de l’ordre du microgramme ou du nanogramme par litre.
De plus, les médicaments sont souvent formulés pour franchir facilement les membranes biologiques, ce qui leur permet d’interagir avec leurs cibles dans une grande diversité d’organismes. Ils doivent également être suffisamment stables pour atteindre ces cibles et exercer leur effet thérapeutique.
En résumé, comme le souligne le rapport de l’OCDE de 2019 consacré à la pollution des eaux douces par les médicaments, « les éléments de conception d’un produit pharmaceutique efficace sont contraires à ce qui est souhaitable dans l’environnement ».
ARGUMENT 2 – Ils représentent une part majeure des micropolluants des eaux usées urbaines
Les résidus de médicaments constituent également un enjeu majeur en raison de la place qu’ils occupent parmi les micropolluants présents dans les eaux usées urbaines.
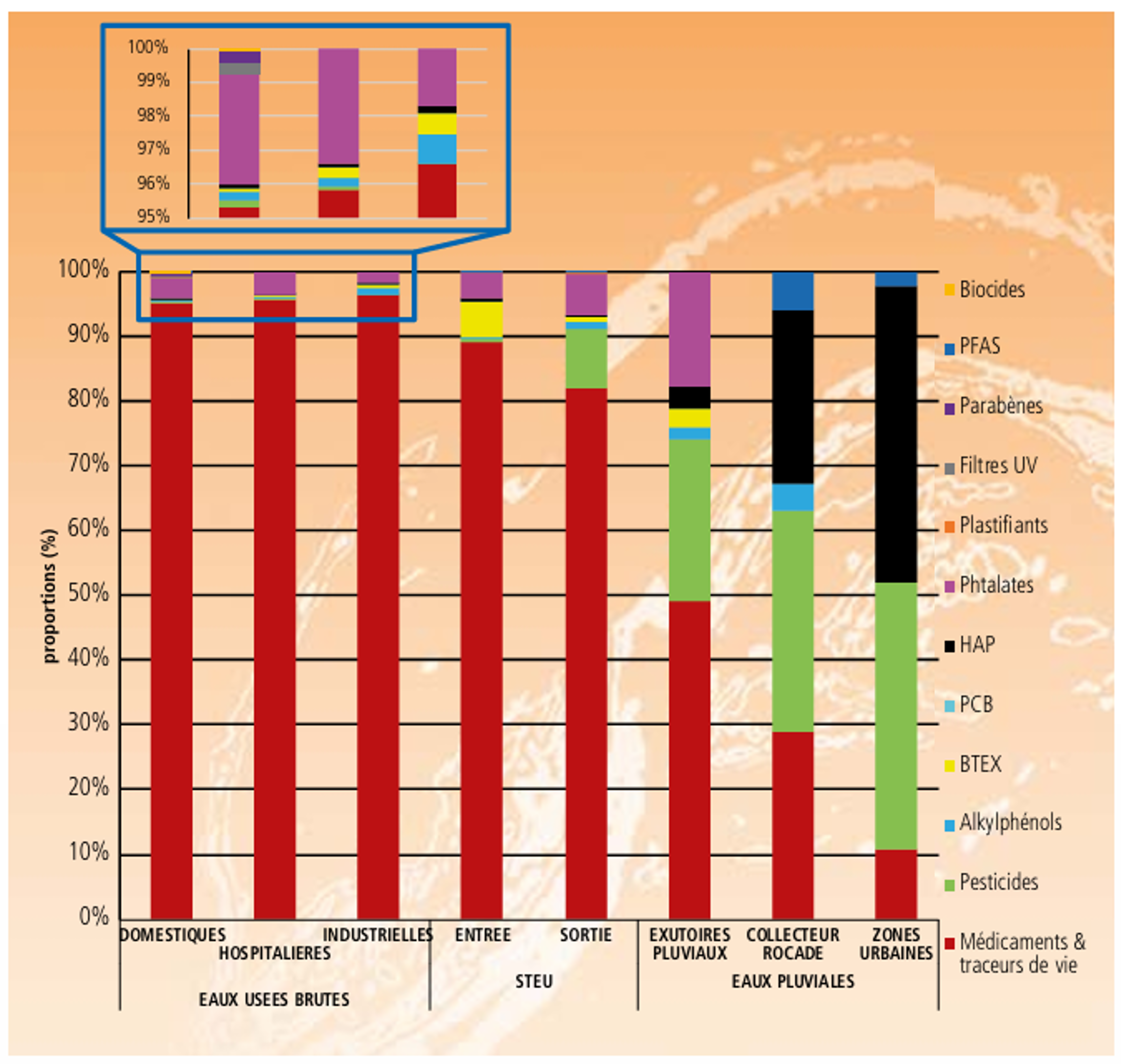
Dans l’agglomération bordelaise, par exemple, les résultats des campagnes de mesures menées sur la station d’épuration locale montrent que les résidus de médicaments peuvent représenter jusqu’à 80 % du flux total de micropolluants détectés dans les eaux usées traitées (Figure 7) (Basilico et al. 2022). Ils arrivent ainsi loin devant les pesticides et les phtalates.
ARGUMENT 3 – Ils sont rejetés tout au long de l’année
Un troisième élément clé est le caractère continu du rejet des résidus de médicaments dans l’environnement.
Pour s’en convaincre, retournons à la station d’épuration de Bellecombe, en Haute-Savoie, avec l’exemple du sulfaméthoxazole (SIPIBEL 2016). Comme l’illustre la Figure 8, les campagnes de mesures réalisées sur les eaux usées urbaines montrent que cet antibiotique est rejeté – car consommé – tout au long de l’année. Des variations existent, avec des pics (par exemple en juin 2015) et des creux (comme en novembre 2013), mais la présence dans les eaux usées reste constante.
En raison de cette émission continue, certaines substances actives pourtant rapidement dégradées dans l’environnement, comme le paracétamol ou l’ibuprofène, sont malgré tout détectées en permanence dans les milieux naturels. Elles sont ainsi qualifiées de pseudo-persistantes.
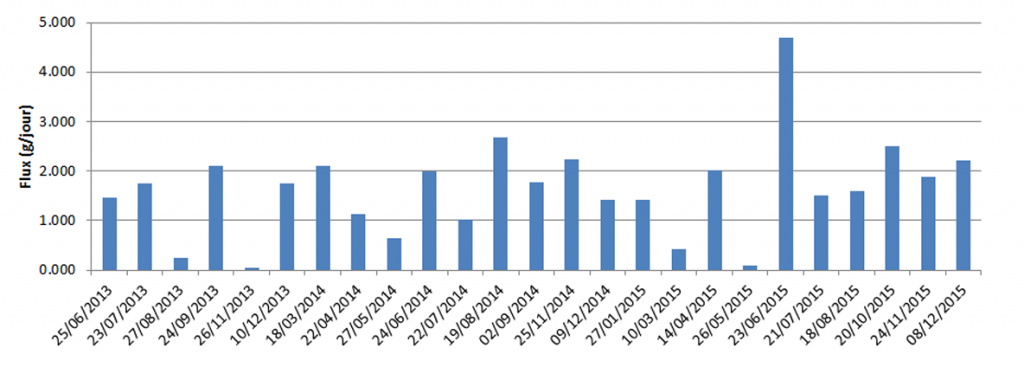
Cette caractéristique distingue les résidus de médicaments d’autres micropolluants comme les pesticides, dont les usages – et donc les rejets – sont fortement saisonniers. Par exemple, les traitements de la vigne se concentrent principalement au printemps.
5. Quels sont les effets des résidus de médicaments sur les organismes vivants ?
5.1 Panorama des effets mesurés lors d’études expérimentales
Les concentrations de résidus de médicaments dans l’environnement sont généralement très faibles. Pour cette raison, ils n’entraînent en règle générale pas de mortalité à court terme chez les organismes exposés. En revanche, ils peuvent induire un large éventail d’effets sublétaux — c’est‑à‑dire des effets qui altèrent le fonctionnement de l’organisme sans provoquer sa mort —, susceptibles, à long terme, de réduire les chances de survie d’un individu ou de compromettre la persistance d’une population.
Ces effets sublétaux sont étudiés de manière intensive depuis le début des années 2000, principalement au moyen d’expérimentations en laboratoire. Le tableau 2 fournit plusieurs exemples d’effets associés à des substances actives appartenant à différents groupes thérapeutiques. Parmi les effets les mieux documentés figurent la perturbation endocrinienne, la reprotoxicité (altération de la reproduction) et les modifications comportementales, en particulier chez les poissons. D’autres effets ont également été observés, tels que la génotoxicité ou l’altération de la croissance.
| Groupe thérapeutique | Effets (et organismes affectés) | Exemples d’études |
| Analgésiques | Dommages aux organes et réduction du succès d’éclosion (poissons) ; Génotoxicité, neurotoxicité et stress oxydatif (mollusques) ; Perturbation hormonale (grenouilles) ; Effets toxiques sur plusieurs niveaux trophiques aquatiques (algues, invertébrés, poissons), incluant altérations physiologiques et biochimiques | (Efosa et al., 2017) ; (Hernandez-Zamora et al., 2025) ; (Mathias et al., 2018) ; (Mezzelani et al., 2016) ; (Näslund et al., 2017) ; (Xia, Zheng et Zhou, 2017) |
| Antibiotiques | Réduction de la croissance (bactéries, algues et plantes aquatiques) ; Effets en cascade sur les bactéries, protozoaires (prédateurs des bactéries), champignons (en compétition avec les bactéries) et les gammares (crustacés) ; Diminution de la production de cocons et dommages à l’ADN (vers de terre) ; Stress oxydatif et altérations enzymatiques (vers de terre) | (Brain et al., 2008) ; (Bundschuh et al., 2009) (Friman et al., 2015 ; (Guo, Boxall et Selby, 2015) (Roose-Amsaleg et Laverman, 2016) ; (Zhai et al., 2025) ; (Zhou et al., 2024) |
| Anticancéreux | Inhibition de la croissance et génotoxicité (micro-organismes et algues), génotoxicité (poissons) | (Araújo et al., 2019) ; (Česen et al., 2016) ; (Novak et al., 2017) ; (Zounková et al., 2007) |
| Antidiabétiques | Perturbation endocrinienne (poissons) | (Crago et al., 2016) ; (Niemuth et al., 2015) |
| Anticonvulsivants | Toxicité pour la reproduction (invertébrés aquatiques) ; Retard de développement (poissons) | (Ferrari et al., 2003) ; (Martinez et al., 2018) |
| Antifongiques | Réduction de la croissance (algues, poissons) ; Perturbation hormonale (rats) | (Porsbring et al., 2009) ; (Stoker, Gibson et Zorrilla, 2010) ; (Vestel et al., 2016) |
| Antihistaminiques | Changements de comportement, croissance et taux d’alimentation (poissons) ; Changements de comportement et toxicité pour la reproduction (invertébrés aquatiques) | (Berninger et al., 2011) ; (Kristofco et al., 2016) ; (Jonsson et al., 2014) ; (Meinertz et al., 2010) |
| Antiparasitaires | Réduction de la croissance et de la reproduction (invertébrés aquatiques) | (Garric et al., 2007) |
| Bêta-bloquants | Comportement reproductif (poissons) ; Toxicité pour la reproduction (invertébrés) | (de Oliveira et al., 2016) ; (Giltrow et al., 2009) |
| Produits hormonaux | Perturbation hormonale entraînant une toxicité pour la reproduction (poissons, grenouilles) | (Armstrong et al., 2016) ; (Gyllenhammar et al., 2009) ; (Kidd et al., 2007*) ; (Kvarnryd et al., 2011) ; (Moore et al., 2016) ; (Nelles, Hu et Prins, 2011) |
| Médicaments à usage psychiatrique | Changements de comportement – alimentation, audace, activité, sociabilité (poissons) ; Perturbation hormonale (poissons) ; Changements de comportement – nage et camouflage (invertébrés aquatiques) ; Toxicité pour la reproduction et perturbation hormonale (invertébrés aquatiques) | (Baskaran Venkatachalam et al., 2023) ; (Brodin et al., 2013 ; 2014) ; (Campos et al., 2016) ; (De Castro-Català et al., 2017) ; (Di Poi et al., 2014) ; (Kellner et al., 2016) ; (Lazzara et al., 2012) ; (Schultz et al., 2011) |
Lire aussi | Les bioessais de laboratoire : évaluer la toxicité des polluants en conditions contrôlées
5.2 Quelques exemples d’études emblématiques
Je vous propose maintenant une incursion dans les laboratoires de recherche pour découvrir quatre exemples emblématiques illustrant les effets des résidus de médicaments sur les organismes vivants.
Exemple 1 : Un anxiolytique qui modifie le comportement des perches [étude en laboratoire]
Cette étude, publiée en 2013 par une équipe de chercheurs de l’Université d’Umeå (Suède) dans la revue Science (Brodin et al. 2013), a largement retenu l’attention des médias. Elle explore les effets de l’oxazépam — un anxiolytique de la famille des benzodiazépines — sur des perches (Perca fluviatilis) exposées pendant sept jours à des concentrations faibles mais réalistes, comparables à celles retrouvées dans les eaux de surface influencées par les rejets d’eaux usées (Figure 8).
L’originalité de ces travaux réside dans le choix des paramètres étudiés. Plutôt que d’évaluer des effets classiques (reproduction, croissance, mortalité), les chercheurs ont analysé quatre traits comportementaux : activité, sociabilité, audace et consommation alimentaire.
Les résultats, illustrés en Figure 9, sont particulièrement marquants. Dès la plus faible dose (1,8 µg/L), les perches exposées sont plus actives (augmentation du nombre d’épisodes de nage), se nourrissent plus rapidement et deviennent moins sociables, c’est-à-dire qu’elles passent moins de temps à proximité de leurs congénères. A dose élevée (910 µg/L), elles deviennent également plus audacieuses, pénétrant plus facilement dans une zone inconnue que les poissons témoins.
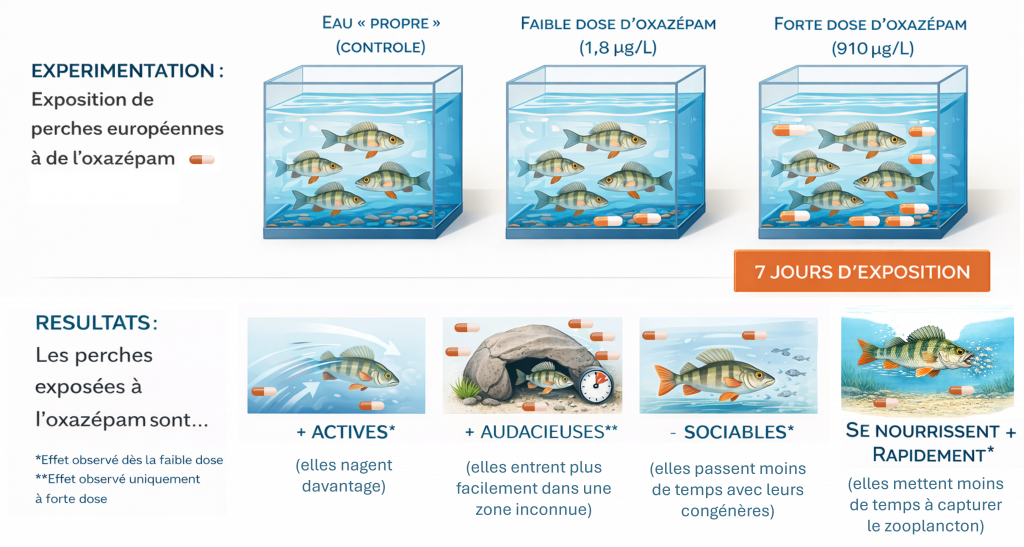
Ces modifications comportementales peuvent sembler anecdotiques. Pourtant, un poisson plus audacieux et moins sociable est probablement plus vulnérable aux prédateurs. Et s’il se nourrit davantage, il exerce une pression accrue sur ses ressources alimentaires.
Ainsi, l’étude conclut que même à très faibles doses, les anxiolytiques rejetés dans l’environnement peuvent avoir des effets significatifs sur la dynamique des populations de poissons et perturber l’équilibre d’un écosystème.
Exemple 2 : Les effets en cascade des antibiotiques sur les communautés microbiennes [études en laboratoire]
Les antibiotiques présents dans les cours d’eau peuvent perturber les micro-organismes qui y vivent. Plusieurs expériences menées sur les bactéries des biofilms — ces fines couches visqueuses qui se développent à la surface des pierres et des plantes aquatiques — montrent que les concentrations retrouvées dans l’environnement peuvent réduire l’abondance des espèces bactériennes les plus sensibles au profit d’espèces plus résistantes (Lecomte et al. 2023b).
Mais ces effets ne s’arrêtent pas là. En modifiant la composition bactérienne, les antibiotiques peuvent également affecter leurs prédateurs naturels. Des travaux ont montré que les bactéries peuvent développer une résistance simultanée aux antibiotiques et aux protozoaires, leurs principaux prédateurs, entraînant un déséquilibre de l’ensemble de la chaîne alimentaire microbienne (Friman et al. 2015).
Parfois, les effets indirects sont plus inattendus. Une étude allemande (Bundschuh et al. 2009) a montré qu’un cocktail d’antibiotiques pouvait favoriser la croissance des champignons sur les feuilles mortes en décomposition, au détriment des bactéries (Figure 10). Ces feuilles, plus riches en champignons, deviennent alors plus appétissantes pour les gammares, de petits crustacés. Autrement dit : les antibiotiques perturbent les bactéries… ce qui favorise les champignons… ce qui modifie le régime alimentaire des crustacés.
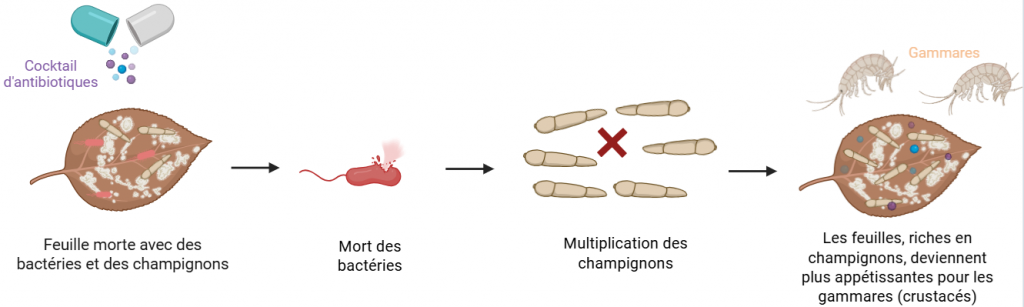
Ces études illustrent bien les effets en cascade que peuvent provoquer les résidus d’antibiotiques dans les milieux aquatiques, avec des répercussions possibles sur la biodiversité et sur le fonctionnement global des écosystèmes.

L’environnement, un réservoir de résistances aux antibiotiques
Selon l’Organisation mondiale de la santé (OMS), la résistance bactérienne aux antibiotiques — appelée aussi antibiorésistance —, constitue l’une des plus graves menaces pour la santé mondiale.
Il est bien connu que l’utilisation abusive ou inappropriée des antibiotiques, chez les humains comme chez les animaux, favorise le développement de l’antibiorésistance. Ce que l’on sait moins, en revanche, c’est que l’environnement pourrait également jouer un rôle dans ce phénomène.
Des bactéries résistantes ont ainsi été détectées dans les eaux usées, mais aussi dans une grande diversité de milieux naturels, notamment en aval des stations d’épuration (Lecomte et al. 2023b). Sous l’effet des activités humaines, ces environnements sont exposés à des résidus d’antibiotiques et à d’autres contaminants chimiques qui, même à faibles concentrations, exercent une pression de sélection sur les microorganismes. Cette pression favorise la survie et la multiplication des bactéries porteuses de gènes de résistance, et peut faciliter l’échange de ces gènes entre bactéries.
L’environnement est ainsi reconnu comme un vaste réservoir de résistances aux antibiotiques. Comprendre ces dynamiques et surveiller leur propagation constitue un enjeu majeur pour préserver l’efficacité des antibiotiques.
Exemple 3 : Une hormone contraceptive qui féminise des poissons mâles [expérimentation à grande échelle]
De nombreuses études ont montré que les résidus d’hormones naturelles ou synthétiques rejetés (notamment) par les stations d’épuration peuvent perturber le développement et la reproduction des poissons d’eau douce.
La plus célèbre est sous doute celle menée dans les années 2000 dans un lac expérimental de l’Ontario (Canada) (Kidd et al. 2007). Pendant sept ans, les chercheurs ont volontairement contaminé le lac avec une faible concentration (5 à 6 ng/L) de 17α-éthynylestradiol, un œstrogène synthétique utilisé dans les pilules contraceptives (Figure 11). L’objectif était d’étudier les effets chroniques (à long terme) de cette hormone sur une population de vairons à grosse tête (Pimephales promelas).
Les résultats sont spectaculaires. Le premier effet mis en évidence correspond à une « féminisation des poissons mâles ». Les scientifiques ont en effet observé chez certains individus une production de vitellogénine, une protéine normalement synthétisée par les femelles lors de la maturation des ovocytes (futurs œufs). Chez certains mâles, ils ont même observé des ovocytes en cours de formation au sein du tissu testiculaire. Surtout, les chercheurs ont constaté un effondrement de la population de vairons, presque éteinte au bout de sept années d’exposition à l’hormone.
Mais les chercheurs ne se sont pas arrêtés à ce sombre constat. Ils ont ensuite cessé de contaminer le lac pour étudier la capacité de rétablissement de la population (Blanchfield et al. 2015). Et c’est la bonne nouvelle : trois ans après l’arrêt de l’exposition, les concentrations de vitellogénine chez les vairons mâles étaient revenues à leur niveau de référence et aucune anomalie testiculaire n’était plus observée. Au printemps de la quatrième année, la population avait retrouvé sa taille initiale (Figure 11).
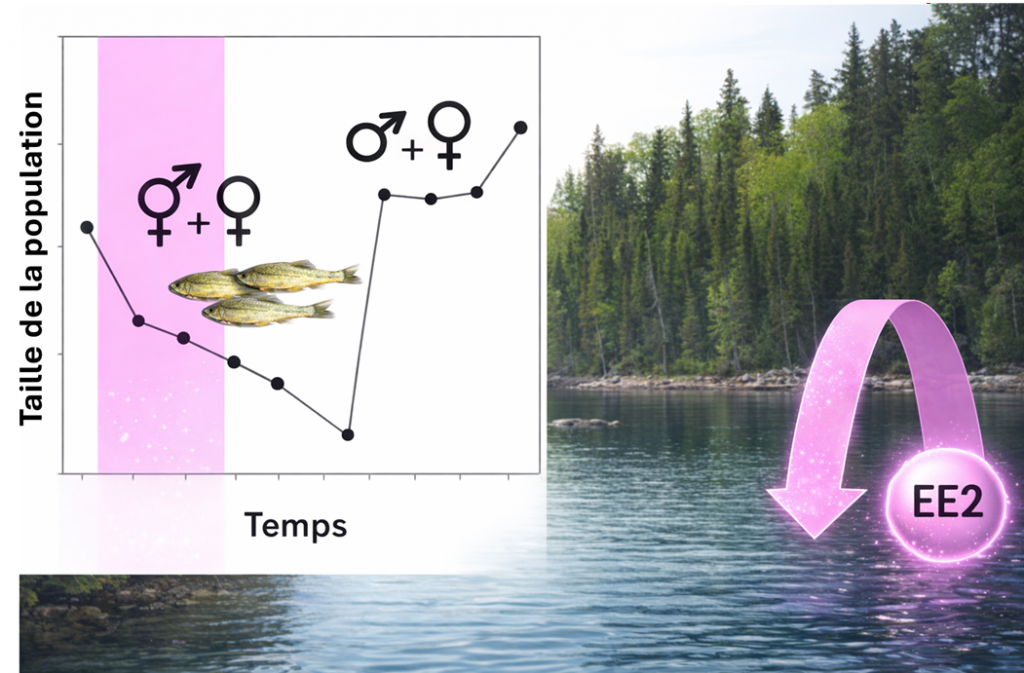
Ces résultats suggèrent à la fois que de faibles concentrations de résidus hormonaux peuvent avoir des effets délétères sur les populations de poissons d’eau douce, et que celles-ci peuvent se rétablir à condition que la source de contamination soit supprimée et que le temps nécessaire à la récupération écologique leur soit laissé.
Exemple 4 : Le diclofénac, responsable de l’effondrement des populations de vautours en Inde et au Pakistan
Je vous ai expliqué précédemment que les résidus de médicaments présents dans l’environnement n’entrainent généralement pas de mortalité à court terme chez les organismes exposés. Le cas des populations de vautours en Inde et au Pakistan constitue un contre-exemple spectaculaire.
A partir des années 1990, ces populations ont connu un véritable effondrement, avec un déclin de plus de 95 % des effectifs en une dizaine d’années seulement (Prakash et al. 2003). Face à cette chute brutale, l’Union internationale pour la conservation de la nature a classé les trois espèces concernées (Gyps bengalensis, Gyps indicus et Gyps tenuirostris) en danger critique d’extinction.
L’origine de cette catastrophe écologique s’est révélée inattendue : le diclofénac . Cet anti-inflammatoire non stéroïdien était alors largement utilisé chez les bovins et les buffles dans le sous-continent indien pour traiter l’inflammation causée par des traumatismes ou des maladies infectieuses. Après la mort des animaux, leurs carcasses sont souvent laissées sur place et constituent une source de nourriture pour les vautours (Photo 6), qui ingèrent alors le médicament présent dans les tissus (Oaks et al. 2004). Or, le diclofénac est extrêmement toxique pour ces oiseaux : même à faible dose, il peut provoquer une insuffisance rénale aiguë mortelle.

Face à l’ampleur de la crise, l’Inde a interdit l’usage vétérinaire du diclofénac en 2006, suivie par le Pakistan en 2010. Depuis, le déclin des populations de vautours a été stoppé, et certaines montrent une lente remontée, même si les effectifs restent très faibles par rapport à la période précédant la crise.
En Europe également, le diclofénac peut représenter une menace pour les vautours. Dans une lettre publiée dans la revue Science en 2021, des scientifiques européens ont exprimé leur inquiétude après l’apparition d’un cas d’intoxication d’un vautour moine en Espagne, où l’usage vétérinaire du diclofénac est autorisé, contrairement à la France.
6. Quel risque font peser les résidus de médicaments sur les écosystèmes ?
6.1 Comment évaluer le risque environnemental ?
Reprenons. Les milieux naturels sont aujourd’hui largement contaminés par des résidus de médicaments ; ces substances ont été conçues pour interagir avec le vivant à faibles doses ; et de nombreux effets ont été observés chez des organismes terrestres et aquatiques, principalement en laboratoire mais aussi sur le terrain. Dans ce contexte, la question du risque que font peser ces résidus de médicaments sur les écosystèmes se pose légitimement.
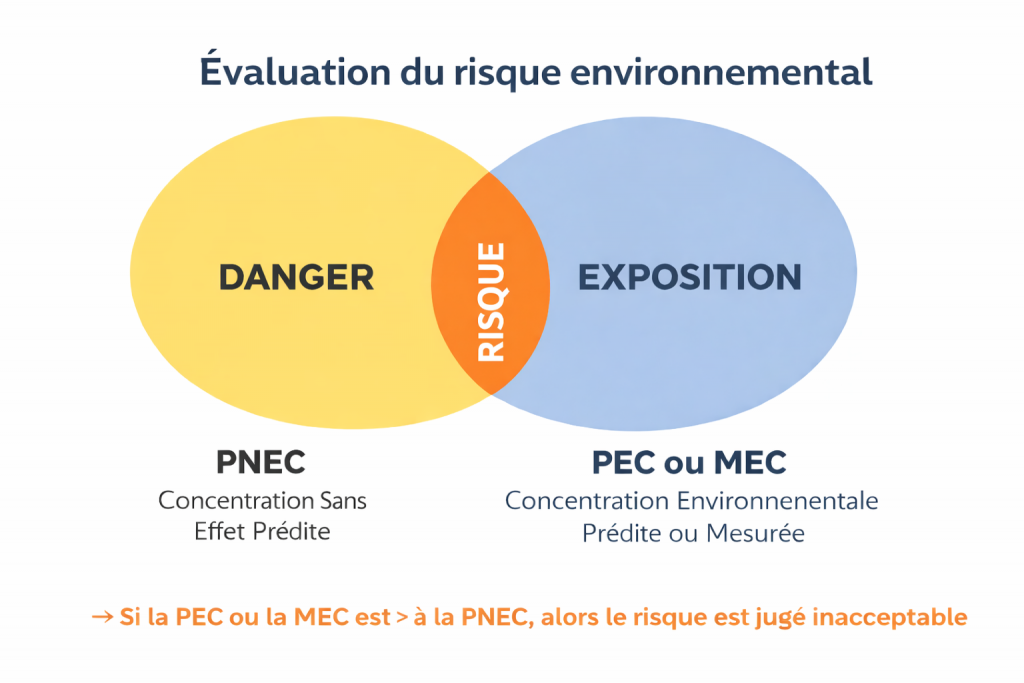
Ce risque « écotoxicologique » repose sur deux composantes essentielles (Figure 12) :
- La dangerosité de la substance, c’est à dire sa toxicité pour les organismes vivants ;
- L’exposition, autrement dit les concentrations auxquelles ces organismes sont exposés dans l’environnement (eau, sédiments, sols, air, etc.).
Pour évaluer concrètement ce risque, on compare :
- les concentrations mesurées dans l’environnement (MEC, Measured Environmental Concentration) ou prédites par des modèles (PEC, Predicted Environmental Concentration),
- à une concentration seuil supposée sans effet (PNEC, Predicted No Effect Concentration), déterminée à partir de tests de toxicité en laboratoire (bioessais) réalisés sur différentes familles d’organismes appartenant à plusieurs niveaux de la chaine alimentaire (par exemple : algues, crustacés et poissons).
En pratique :
- si la concentration mesurée ou prédite dépasse la PNEC, un risque est suspecté (risque « élevé » ou « inacceptable ») ;
- si elle est inférieure, le risque est considéré comme acceptable.
Cette démarche est utilisée dans le cadre d’une autorisation de mise sur le marché (AMM) d’un nouveau médicament (voir encadré plus bas), mais aussi dans le cadre de programmes de surveillance et de travaux de recherche.
Comment le risque environnemental est-il pris en compte dans l’AMM d’un médicament ?
En Europe, tous les médicaments — qu’ils soient destinés à l’humain (Directive 2001/83/CE) ou aux animaux (Directive 2001/82/CE et Règlement (UE) 2019/6) — font l’objet d’une évaluation du risque environnemental (ERE) avant leur autorisation de mise sur le marché. Mais sa prise en compte dans la décision diffère fortement. Pour les médicaments humains, l’ERE est non bloquante : même en cas de risque environnemental identifié, le médicament peut être autorisé si son bénéfice pour les patients est jugé suffisant. Pour les médicaments vétérinaires, en revanche, l’environnement est pleinement intégré dans la balance bénéfice/risque : un risque jugé inacceptable peut conduire à un refus d’AMM ou à des restrictions d’usage.
Dans les deux cas, l’ERE n’est pas rétroactive, ce qui exclue de fait la majorité des médicaments actuellement sur le marché. Beaucoup de médicaments « anciens » restent donc non évalués, même si certaines évaluations peuvent être demandées au cas par cas.
Lire aussi | Méthode d’évaluation du risque environnemental d’une substance chimique
6.2 Les seuils de risque sont parfois dépassés
Les évaluations disponibles montrent que ces seuils sont parfois dépassés.
A l’échelle mondiale, l’étude de Wilkinson et al. (2022) révèle que les concentrations de substances actives excèdent les seuils à risque pour les organismes aquatiques dans environ un quart des sites étudiés. Le sulfaméthoxazole (antibiotique) est la substance dont la concentration dépasse le plus souvent la PNEC (140 sites sur 1 052).
Une autre étude, basée sur une compilation des données de contamination des boues de station d’épuration et composts disponibles dans la littérature scientifique internationale, montre que les sols amendés par ces matières fertilisantes peuvent présenter un risque lié à certaines substances, notamment la ciprofloxacine et les œstrogènes 17α-ethinylestradiol et 17β-estradiol (Mejías et al. 2021).
En France, une évaluation du risque écotoxicologique menée dans le cadre du programme de surveillance de l’agence de l’eau Seine-Normandie met en évidence des dépassements de PNEC pour le diclofénac et l’ibuprofène. Ces dépassements sont particulièrement localisés en Île-de-France, le long de l’axe Seine et dans certaines petites rivières urbaines.
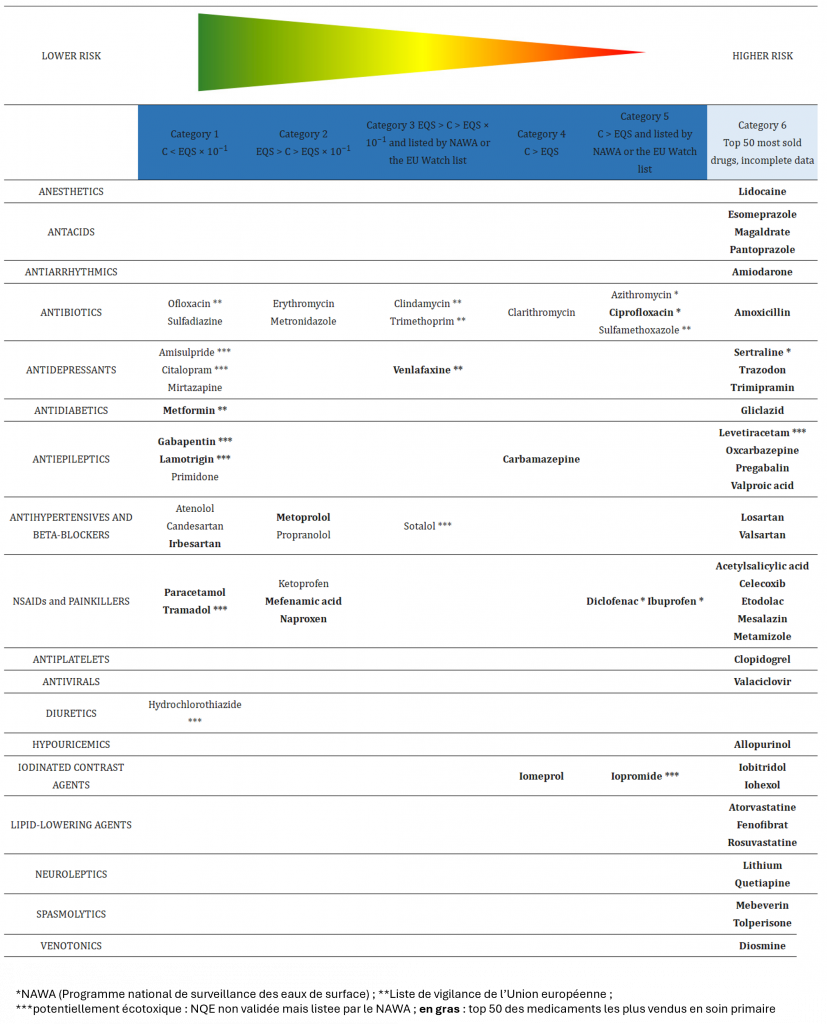
En Suisse, une étude du centre universitaire de médecine générale et santé publique de Lausanne a classé les substances actives les plus vendues selon leur risque environnemental (Charmillot et al. 2025). Les résultats (Figure 13), identifient les substances les plus problématiques pour les milieux aquatiques, au sein de chaque classe thérapeutique.
Par exemple, parmi les antibiotiques, l’azythromycine, la ciprofloxacine et le sulfaméthoxazole présentent un risque élevé, tandis que l’ofloxacine et la sulfadiazine présentent un risque faible.
6.3 De nombreuses inconnues persistent
Plus largement, le niveau d’impact global des résidus de médicaments sur la biodiversité reste difficile à établir. Et ce, pour trois raisons principales.
Le manque de données constitue un premier obstacle majeur. Plus de 3 500 substances actives à usage pharmaceutique sont actuellement commercialisées dans le monde. Or, pour une grande partie d’entre elles, les données de toxicité environnementale sont incomplètes ou inaccessibles au public (OECD 2019). Et ce, sans même considérer les métabolites, pour lesquels les données sont encore plus rares. De plus, la majorité de ces substances ne font pas l’objet d’un suivi régulier dans l’environnement.
Pour ces raisons, dans l’étude suisse mentionnée plus haut, l’évaluation du risque a été impossible pour 34 des 50 substances actives les plus vendues dans le pays (Figure 13).
Un deuxième facteur limitant de l’évaluation du risque est lié à ce que l’on appelle les effets « cocktails ». Dans les milieux naturels, les organismes (poissons, algues, vers de terre, etc.) ne sont pas exposés à une seule substance, mais à des mélanges complexes pouvant contenir plusieurs centaines voire plusieurs milliers de substances (médicaments, métaux, pesticides, PFAS, etc.). Les effets de celles-ci peuvent s’additionner (effets additifs), se renforcer (effets synergiques) ou, au soustraire, s’atténuer (effets antagonistes). Ces interactions, difficiles à prédire, restent encore largement absentes des cadres réglementaires.

Enfin, la pollution chimique ne constitue qu’une pression parmi d’autres. Les écosystèmes sont aussi affectés par la destruction des habitats, la propagation d’espèces invasives ou encore le changement climatique. De plus, les effets des résidus de médicaments (et des autres micropolluants) peuvent varier selon les conditions environnementales, telles que la saison, la température ou la disponibilité en nutriments (Lecomte et al. 2023b).
Dans ce contexte, il est particulièrement difficile de démontrer, sur le terrain, des relations de causalité directes entre la présence de résidus de médicaments et des effets chroniques à long terme sur les écosystèmes. Des études écologiques à grande échelle sont donc nécessaires pour objectiver ces impacts.
Ces incertitudes ne doivent toutefois pas conduire à l’inaction. Elles invitent au contraire les pouvoirs publics, les industries pharmaceutiques, les professionnels de santé, les acteurs de l’eau et les citoyens à agir dès à présent pour limiter cette pollution.
… et ce sera précisément l’objet de mon prochain article 😉
Article rédigé par Vivien Lecomte, 14 avril 2026 – Ecotoxicologie.fr : tous droits réservés
EN SAVOIR PLUS
Basilico, L., E. Villemagne & P.-F. Staub 2022 Micropolluants émis par le secteur de la santé : prendre soin aussi de l’eau – Retours d’expériences et recommandation à l’intention des acteurs hospitaliers et de la santé, Office français de la biodiversité (OFB) – https://www.documentation.eauetbiodiversite.fr/fr/notice/micropolluants-emis-par-le-secteur-de-la-sante-prendre-soin-aussi-de-l-eau-retours-d-experiences-et-recommandations-a-l-intention-des-acteurs-hospitaliers-et-de-la-sante-29191
Dagot, C. 2018 « Traitement des résidus de médicaments dans les ouvrages d’épuration des eaux », Environnement, Risques & Santé 17.1 : 47-58. doi : 10.1684/ers.2017.1126.
Etienne, N. 2024 Transferts et processus associés aux résidus de médicaments humains et vétérinaires et aux biocides des boues urbaines et des lisiers utilisés comme fertilisants, Thèses, INSA Lyon. https://hal.science/tel-04684348.
Lecomte, V., J. Artigas, C. Bonnineau, E. Brelot, C. Dagot, D. Hocquet, J. Labanowski, C. Miege, L. Mondamert, F. Martin-Laurent & S. Pesce 2023 « Contamination des milieux aquatiques par les résidus de médicaments : exposition, risques écotoxicologiques, antibiorésistance et leviers d’actions », Environnement, Risques & Santé 22.5 : 359-375. doi : 10.1684/ers.2023.1754.
OECD 2019 Pharmaceutical Residues in Freshwater: Hazards and Policy Responses, Paris : OECD publishing : 138. doi : https://doi.org/10.1787/c936f42d-en.
Wilkinson, J. L., et al. 2022 « Pharmaceutical Pollution of the World’s Rivers », Proceedings of the National Academy of Sciences of the United States of America 119.8 : e2113947119. doi : 10.1073/pnas.2113947119.
REFERENCES BIBLIOGRAPHIQUES
ADEME Pays-de-la-Loire 2018 Matières fertilisantes organiques : gestion et épandage – Guide des bonnes pratiques, ADEME (« Clés pour Agir »). https://librairie.ademe.fr/economie-circulaire-et-dechets/1505-matieres-fertilisantes-organiques-gestion-et-epandage-9791029709845.html : 15.
Agence de l’eau Adour-Garonne & OFB 2022 « [Restitution] Colloque Micropolluants dans l’eau, un enjeu pour le vivant », Le portail technique de l’OFB. https://professionnels.ofb.fr/fr/restitution/restitution-colloque-micropolluants-dans-leau-enjeu-vivant.
Agence de l’eau Seine Normandie 2026 Le point sur la contamination par les résidus médicamenteux sur le bassin Seine-Normandie, Agence de l’eau Seine Normandie (AESN) (« Le point sur… »). https://www.eau-seine-normandie.fr/actualites/le_point_sur_la_contamination_par_les_residus_medicamenteux_sur_le_bassin_seine_normandie : 22.
Amouroux, I., J.-L. Gonzalez, A. Grouhel, F. Chavanon, S. Augagneur, A. Bruneau, H. Budzinski, F. Dagault, V. Duquesne, R. Gabellec, F. Le Bon, L. Lebrun, I. Le Fur, P. Le Gall, C. Gianaroli, M. Lissardy, F. Maheux, D. Munaron, O. Pierre Duplessix, C. Ravel, M. Retho, A. Schmidt, B. Simon, T. Sireau, P.-F. Staub, N. Tapie, A. Thevand, A. Grouhel, F. Chavanon, S. Augagneur, A. Bruneau, H. Budzinski, F. Dagault, V. Duquesne, R. Gabellec, F. Le Bon, L. Lebrun, I. Le Fur, P. Le Gall, C. Gianaroli, M. Lissardy, F. Maheux, D. Munaron, O. Pierre Duplessix, C. Ravel, M. Retho, A. Schmidt, B. Simon, T. Sireau, P.-F. Staub, N. Tapie & A. Thevand 2025 « Emergent’Sea. Recherche des substances d’intérêt émergent en milieu marin ». https://archimer.ifremer.fr/doc/00956/106772/.
ANSES 2020 Antibiorésistance et environnement – État et causes possibles de la contamination des milieux en France. https://www.anses.fr/fr/system/files?file=EAUX2016SA0252Ra.pdf : 298.
Basilico, L., E. Villemagne & P.-F. Staub 2022 Micropolluants émis par le secteur de la santé : prendre soin aussi de l’eau – Retours d’expériences et recommandation à l’intention des acteurs hospitaliers et de la santé, Office francçais de la biodiversité (OFB) (« Comprendre pour agir » N°44). https://www.documentation.eauetbiodiversite.fr/fr/notice/micropolluants-emis-par-le-secteur-de-la-sante-prendre-soin-aussi-de-l-eau-retours-d-experiences-et-recommandations-a-l-intention-des-acteurs-hospitaliers-et-de-la-sante-29191 : 28.
Benotti, M. J. & B. J. Brownawell 2009 « Microbial degradation of pharmaceuticals in estuarine and coastal seawater », Environmental Pollution 157.3 : 994-1002. doi : 10.1016/j.envpol.2008.10.009.
Biel-Maeso, M., C. Corada-Fernández & P. A. Lara-Martín 2018 « Monitoring the occurrence of pharmaceuticals in soils irrigated with reclaimed wastewater », Environmental Pollution 235 : 312-321. doi : 10.1016/j.envpol.2017.12.085.
BIO Intelligence Service 2013 Study on the environmental risks of medicinal products, Final Report prepared for Executive Agency for Health and Consulmers. https://health.ec.europa.eu/document/download/592edea4-27d9-4b36-933a-6009057960c1_en : 310.
Blanchfield, P. J., K. A. Kidd, M. F. Docker, V. P. Palace, B. J. Park & L. D. Postma 2015 « Recovery of a Wild Fish Population from Whole-Lake Additions of a Synthetic Estrogen », Environmental Science & Technology 49.5 : 3136-3144. doi : 10.1021/es5060513.
Brodin, T., J. Fick, M. Jonsson & J. Klaminder 2013 « Dilute Concentrations of a Psychiatric Drug Alter Behavior of Fish from Natural Populations », Science 339.6121 : 814-815. doi : 10.1126/science.1226850.
Bundschuh, M., T. Hahn, M. O. Gessner & R. Schulz 2009 « Antibiotics as a Chemical Stressor Affecting an Aquatic Decomposer-Detritivore System », Environmental Toxicology and Chemistry 28.1 : 197-203. doi : 10.1897/08-075.1.
Carballo, M., S. Aguayo, M. González, F. Esperon & A. de la Torre 2016 « Environmental Assessment of Tetracycline’s Residues Detected in Pig Slurry and Poultry Manure », Journal of Environmental Protection 7.1 : 82-92. doi : 10.4236/jep.2016.71008.
Cemagref 2009 Synthèse du projet ANR AMPERES : Analyse de micropolluants prioritaires et émergents dans les rejets et les eaux superficielles (2006 – 2009). https://www.eauxglacees.com/IMG/pdf/1._AMPERES_synthese_2009.pdf : 6.
Charmillot, T., N. Chèvre & N. Senn 2025 « Developing an Ecotoxicological Classification for Frequently Used Drugs in Primary Care », International Journal of Environmental Research and Public Health 22.2 : 290. doi : 10.3390/ijerph22020290.
Dagot, C. 2018 « Traitement des résidus de médicaments dans les ouvrages d’épuration des eaux », Environnement, Risques & Santé 17.1 : 47-58. doi : 10.1684/ers.2017.1126.
Deschamps, M., S. Ferhi, N. Bernet, F. Feder, O. Crouzet, D. Steyer, D. Montenach, G. D. Moussard, V. Lamoureux, P. Benoit & S. Houot 2017 « Effets d’apports répétés de PROs au champ sur les teneurs en composés pharmaceutiques dans les sols et risques ecotoxicologiques associés ». https://hal.science/hal-01606093 : np.
Etienne, N. 2024 Transferts et processus associés aux résidus de médicaments humains et vétérinaires et aux biocides des boues urbaines et des lisiers utilisés comme fertilisants, Theses, INSA Lyon. https://hal.science/tel-04684348.
Etienne, N., J.-P. Bedell, J.-L. Bertrand-Krajewski, P. Benoit, E. Brelot, C. Dagot, D. Patureau, A. Pinscloux & L. Wiest 2024 Synthèse du programme RISMEAU – Risques liés aux résidus des médicaments, biocides et antibiorésistance d’origine humaine et vétérinaire sur les ressources en eau du bassin de l’Arve. Développé en appui sur le site pilote de Bellecombe SIPIBEL (2019 – 2023). https://www.graie.org/graie/graiedoc/doc_telech/actesyntheses/Synthese_Programme_Rismeau_2019_2023.pdf.
Fernandes, J. P., C. M. R. Almeida, M. A. Salgado, M. F. Carvalho & A. P. Mucha 2021 « Pharmaceutical Compounds in Aquatic Environments—Occurrence, Fate and Bioremediation Prospective », Toxics 9.10. doi : 10.3390/toxics9100257.
Friman, V.-P., L. M. Guzman, D. C. Reuman & T. Bell 2015 « Bacterial adaptation to sublethal antibiotic gradients can change the ecological properties of multitrophic microbial communities », Proceedings of the Royal Society B: Biological Sciences 282.1806 : 20142920. doi : 10.1098/rspb.2014.2920.
Gworek, B., M. Kijeńska, J. Wrzosek & M. Graniewska 2021 « Pharmaceuticals in the Soil and Plant Environment: A Review », Water, Air, & Soil Pollution 232.4 : 145. doi : 10.1007/s11270-020-04954-8.
INRA, CNRS & IRSTEA 2014 Valorisation des matières fertilisantes d’origine résiduaire sur les sols à usage agricole ou forestier : impacts agronomiques, environnementaux socio-économiques – Synthèse de l’expertise scientifique collective. https://www.inrae.fr/sites/default/files/pdf/mafor-synthese-vf-oct2014.pdf : 108.
INRAE & Graie 2022 « Séminaire Pharma Aqua », in Contamination des milieux aquatiques par les substances pharmaceutiques. Impacts sur l’environnement et risques sur la santé, Annecy. https://asso.graie.org/portail/actes-pharma-aqua-science-et-societe/.
Kalinski, J.-C. J., A. K. Pakkir Mohamed Shah, B. Ruiz Brandão da Costa, S. P. Farrell, L. Schellenberg, L. G. Graves, T. Schramm, P. Stincone, I. Koester, B. M. Stephens, R. R. Torres, L. Cancelada, C. Utermann-Thüsing, Z. A. Quinlan, L. Wegley Kelly, C. A. Carlson, C. Castillo-Ilabaca, S. Pantoja-Gutiérrez, J. M. Beman, A. Hartmann, A. Aron, X. Siwe Noundou, R. A. Dorrington, D. Tasdemir, A. F. Haas, P. C. Dorrestein, C. E. Nelson, L. I. Aluwihare, M. Wang & D. Petras 2026 « Widespread Presence of Anthropogenic Compounds in Marine Dissolved Organic Matter », Nature Geoscience : 1-10. doi : 10.1038/s41561-026-01928-z.
Kidd, K. A., P. J. Blanchfield, K. H. Mills, V. P. Palace, R. E. Evans, J. M. Lazorchak & R. W. Flick 2007 « Collapse of a Fish Population after Exposure to a Synthetic Estrogen », Proceedings of the National Academy of Sciences of the United States of America 104.21 : 8897-8901. doi : 10.1073/pnas.0609568104.
Larsson, D. G. J. 2014 « Pollution from drug manufacturing: review and perspectives », Philosophical Transactions of the Royal Society B: Biological Sciences 369.1656 : 20130571. doi : 10.1098/rstb.2013.0571.
Larsson, D. G. J., C. de Pedro & N. Paxeus 2007 « Effluent from drug manufactures contains extremely high levels of pharmaceuticals », Journal of Hazardous Materials 148.3 : 751-755. doi : 10.1016/j.jhazmat.2007.07.008.
Lecomte, V., J.-L. Bertrand-Krajewski, A. Bouchez, B. Cournoyer, C. Dagot, A. Gonzalez-Ospina, J. Labanowski, Y. Lévi, Y. Perrodin & L. Wiest 2018 « SIPIBEL : un site pilote pour l’étude des effluents hospitaliers et urbains. Les grands enseignements après cinq ans de suivi et de recherche », Environnement, Risques & Santé 17.1 : 59-74. doi : 10.1684/ers.2017.1074.
Lecomte, V., O. Geffard, M. Coquery & C. Miege 2023a La biosurveillance active à l’aide de l’amphipode Gammarus fossarum : optimiser et élargir la liste des substances d’intérêt à rechercher, INRAE Lyon-Grenoble-Auvergne-Rhône-Alpes ; Office français de la biodiversité (OFB). https://hal.science/hal-04567636.
Lecomte, V., J. Artigas, C. Bonnineau, E. Brelot, C. Dagot, D. Hocquet, J. Labanowski, C. Miege, L. Mondamert, F. Martin-Laurent & S. Pesce 2023b « Contamination des milieux aquatiques par les résidus de médicaments : exposition, risques écotoxicologiques, antibiorésistance et leviers d’actions », Environnement, Risques & Santé 22.5 : 359-375. doi : 10.1684/ers.2023.1754.
leem (les entreprises du médicament) 2024 Bilan économique des entreprises du médicament – Edition 2024, leem. https://www.leem.org/publication/bilan-economique-des-entreprises-du-medicament-edition-2024 : 96.
Li, Z., A. Sobek & M. Radke 2016 « Fate of Pharmaceuticals and Their Transformation Products in Four Small European Rivers Receiving Treated Wastewater », Environmental Science & Technology 50.11 : 5614-5621. doi : 10.1021/acs.est.5b06327.
Lin, A. Y.-C., C.-A. Lin, H.-H. Tung & N. S. Chary 2010 « Potential for biodegradation and sorption of acetaminophen, caffeine, propranolol and acebutolol in lab-scale aqueous environments », Journal of Hazardous Materials 183.1 : 242-250. doi : 10.1016/j.jhazmat.2010.07.017.
Mejías, C., J. Martín, J. L. Santos, I. Aparicio & E. Alonso 2021 « Occurrence of pharmaceuticals and their metabolites in sewage sludge and soil: A review on their distribution and environmental risk assessment », Trends in Environmental Analytical Chemistry 30 : e00125. doi : 10.1016/j.teac.2021.e00125.
Murgatroyd, O., L. Petrik, C. Y. Ojemaye & D. Pillay 2025 « Persistent Pharmaceuticals in a South African Urban Estuary and Bioaccumulation in Endobenthic Sandprawns (Kraussillichirus Kraussi) », Water 17.15. doi : 10.3390/w17152289.
Oaks, J. L., M. Gilbert, M. Z. Virani, R. T. Watson, C. U. Meteyer, B. A. Rideout, H. L. Shivaprasad, S. Ahmed, M. J. Iqbal Chaudhry, M. Arshad, S. Mahmood, A. Ali & A. Ahmed Khan 2004 « Diclofenac Residues as the Cause of Vulture Population Decline in Pakistan », Nature 427.6975 : 630-633. doi : 10.1038/nature02317.
OECD 2019 Pharmaceutical Residues in Freshwater: Hazards and Policy Responses, Paris : OECD publishing (« OECD Studies on Water »). : 138. doi : https://doi.org/10.1787/c936f42d-en.
Paltiel, O., G. Fedorova, G. Tadmor, G. Kleinstern, Y. Maor & B. Chefetz 2016 « Human Exposure to Wastewater-Derived Pharmaceuticals in Fresh Produce: A Randomized Controlled Trial Focusing on Carbamazepine », Environmental Science & Technology 50.8 : 4476-4482. doi : 10.1021/acs.est.5b06256.
Posselt, M., J. Mechelke, C. Rutere, C. Coll, A. Jaeger, M. Raza, K. Meinikmann, S. Krause, A. Sobek, J. Lewandowski, M. A. Horn, J. Hollender & J. P. Benskin 2020 « Bacterial Diversity Controls Transformation of Wastewater-Derived Organic Contaminants in River-Simulating Flumes », Environmental Science & Technology 54.9 : 5467-5479. doi : 10.1021/acs.est.9b06928.
Poterszman, B. & H. Pouzet 2026 Médicaments : d’où viennent les pénuries ?, (« Les docs de La Fabrique, Presses des Mines »). https://www.la-fabrique.fr/fr/publication/medicaments-dou-viennent-les-penuries/
Prakash, V., D. J. Pain, A. A. Cunningham, P. F. Donald, N. Prakash, A. Verma, R. Gargi, S. Sivakumar & A. R. Rahmani 2003 « Catastrophic collapse of Indian white-backed Gyps bengalensis and long-billed Gyps indicus vulture populations », Biological Conservation 109.3 : 381-390. doi : 10.1016/S0006-3207(02)00164-7.
Schapira, M., O. Manor, N. Golan, D. Kalo, V. Mordehay, N. Kirshenbaum, R. Goldsmith, B. Chefetz & O. Paltiel 2020 « Involuntary Human Exposure to Carbamazepine: A Cross-Sectional Study of Correlates across the Lifespan and Dietary Spectrum », Environment International 143 : 105951. doi : 10.1016/j.envint.2020.105951.
SIPIBEL 2016 SIPIBEL – Rapport 2011-2015 – Résultats de quatre années de suivi, d’études et de recherches sur le site pilote de Bellecombe, Graie. https://graie.org/Sipibel/publications/sipibel-rapport-effluentshospitaliersmedicaments-oct16.pdf : 174.
Terzic, S., K. Ivankovic, K. Jambrosic, B. Kurtovic & M. Ahel 2024 « Bioaccumulation and tissue distribution of pharmaceuticals and their transformation products in fish along the pollution gradients of a wastewater-impacted river », Science of The Total Environment 956 : 177339. doi : 10.1016/j.scitotenv.2024.177339.
Thiebault, T. 2024 Les produits pharmaceutiques dans les environnements anthropisés, de la mesure de la contamination à l’information sur les usages, Accreditation to supervise research, Ecole Pratique des Hautes Etudes. https://hal.science/tel-04720770.
Wilkinson, J. L., A. B. A. Boxall, D. W. Kolpin, K. M. Y. Leung, R. W. S. Lai, C. Galbán-Malagón, A. D. Adell, J. Mondon, M. Metian, R. A. Marchant, A. Bouzas-Monroy, A. Cuni-Sanchez, A. Coors, P. Carriquiriborde, M. Rojo, C. Gordon, M. Cara, M. Moermond, T. Luarte, V. Petrosyan, Y. Perikhanyan, C. S. Mahon, C. J. McGurk, T. Hofmann, T. Kormoker, V. Iniguez, J. Guzman-Otazo, J. L. Tavares, F. Gildasio De Figueiredo, M. T. P. Razzolini, V. Dougnon, G. Gbaguidi, O. Traoré, J. M. Blais, L. E. Kimpe, M. Wong, D. Wong, R. Ntchantcho, J. Pizarro, G.-G. Ying, C.-E. Chen, M. Páez, J. Martínez-Lara, J.-P. Otamonga, J. Poté, S. A. Ifo, P. Wilson, S. Echeverría-Sáenz, N. Udikovic-Kolic, M. Milakovic, D. Fatta-Kassinos, L. Ioannou-Ttofa, V. Belušová, J. Vymazal, M. Cárdenas-Bustamante, B. A. Kassa, J. Garric, A. Chaumot, P. Gibba, I. Kunchulia, S. Seidensticker, G. Lyberatos, H. P. Halldórsson, M. Melling, T. Shashidhar, M. Lamba, A. Nastiti, A. Supriatin, N. Pourang, A. Abedini, O. Abdullah, S. S. Gharbia, F. Pilla, B. Chefetz, T. Topaz, K. M. Yao, B. Aubakirova, R. Beisenova, L. Olaka, J. K. Mulu, P. Chatanga, V. Ntuli, N. T. Blama, S. Sherif, A. Z. Aris, L. J. Looi, M. Niang, S. T. Traore, R. Oldenkamp, O. Ogunbanwo, M. Ashfaq, M. Iqbal, Z. Abdeen, A. O’Dea, J. M. Morales-Saldaña, M. Custodio, H. de la Cruz, I. Navarrete, F. Carvalho, A. B. Gogra, B. M. Koroma, V. Cerkvenik-Flajs, M. Gombač, M. Thwala, K. Choi, H. Kang, J. L. C. Ladu, A. Rico, P. Amerasinghe, A. Sobek, G. Horlitz, A. K. Zenker, A. C. King, J.-J. Jiang, R. Kariuki, M. Tumbo, U. Tezel, T. T. Onay, J. B. Lejju, Y. Vystavna, Y. Vergeles, H. Heinzen, A. Pérez-Parada, D. B. Sims, M. Figy, D. Good & C. Teta 2022 « Pharmaceutical Pollution of the World’s Rivers », Proceedings of the National Academy of Sciences of the United States of America 119.8 : e2113947119. doi : 10.1073/pnas.2113947119.
Winker, M., J. Clemens, M. Reich, H. Gulyas & R. Otterpohl 2010 « Ryegrass uptake of carbamazepine and ibuprofen applied by urine fertilization », Science of The Total Environment 408.8 : 1902-1908. doi : 10.1016/j.scitotenv.2010.01.028.
Zind, H., L. Mondamert, Q. Blancart-Remaury, A. Cleon, N. K. V. Leitner & J. Labanowski 2021 « Occurrence of carbamazepine, diclofenac, and their related metabolites and transformation products in a French aquatic environment and preliminary risk assessment », Water Research 196 : 117052. doi : 10.1016/j.watres.2021.117052.
Directive 2001/82/CE du Parlement européen et du Conseil instituant un code communautaire relatif aux médicaments vétérinaires 2001 . doi : https://eur-lex.europa.eu/legal-content/FR/TXT/HTML/?uri=CELEX:32001L0082.
Directive 2001/83/CE du Parlement européen et du Conseil du 6 novembre 2001 instituant un code communautaire relatif aux médicaments à usage humain 2001 . https://eur-lex.europa.eu/legal-content/FR/TXT/HTML/?uri=CELEX:32001L0083.
Règlement (UE) 2019/6 du Parlement européen et du Conseil du 11 décembre 2018 relatif aux médicaments vétérinaires et abrogeant la directive 2001/82/CE (Texte présentant de l’intérêt pour l’EEE) 2018 . https://eur-lex.europa.eu/legal-content/FR/TXT/?uri=CELEX:32019R0006.






 Il se vend près de 6 shampoings chaque seconde en France soit près de 200 millions de bouteilles par an
Il se vend près de 6 shampoings chaque seconde en France soit près de 200 millions de bouteilles par an Les produits d’entretien classiques contiennent des tensioactifs (appelés aussi agents de surface ou détergents) qui permettent d’éliminer les graisses et autres salissures à la surface de matériaux. Les détergents anioniques (charge négative) et amphotériques (dont la charge dépend du pH de l’eau) sont particulièrement présents dans les produits nettoyants, en raison de leurs propriétés nettoyantes et moussantes
Les produits d’entretien classiques contiennent des tensioactifs (appelés aussi agents de surface ou détergents) qui permettent d’éliminer les graisses et autres salissures à la surface de matériaux. Les détergents anioniques (charge négative) et amphotériques (dont la charge dépend du pH de l’eau) sont particulièrement présents dans les produits nettoyants, en raison de leurs propriétés nettoyantes et moussantes  Les phtalates, produits à quelque 6 millions de tonnes par an dans le monde
Les phtalates, produits à quelque 6 millions de tonnes par an dans le monde  20 millions de lave-linge tournent en France chaque jour en moyenne
20 millions de lave-linge tournent en France chaque jour en moyenne  La France est le 4ème consommateur mondial de médicaments : plus de 3000 médicaments à usage humain et 300 médicaments vétérinaires sont actuellement disponibles sur le marché français. Une fois que ces substances ont agi dans l’organisme, elles sont excrétées, essentiellement dans les selles et les urines, puis relarguées dans les réseaux d’eaux usées (médicaments humains) et dans les sols (médicaments vétérinaires). Une partie de ces résidus de médicaments se retrouvent donc d’une manière ou d’une autre dans le milieu aquatique. Des traces de ces composés sont d’ailleurs régulièrement détectées dans les eaux de surface et même dans les eaux de nappe
La France est le 4ème consommateur mondial de médicaments : plus de 3000 médicaments à usage humain et 300 médicaments vétérinaires sont actuellement disponibles sur le marché français. Une fois que ces substances ont agi dans l’organisme, elles sont excrétées, essentiellement dans les selles et les urines, puis relarguées dans les réseaux d’eaux usées (médicaments humains) et dans les sols (médicaments vétérinaires). Une partie de ces résidus de médicaments se retrouvent donc d’une manière ou d’une autre dans le milieu aquatique. Des traces de ces composés sont d’ailleurs régulièrement détectées dans les eaux de surface et même dans les eaux de nappe  On estime que 4000 à 6000 tonnes d’écran total sont libérées chaque année dans les zones de récifs tropicales par les 78 millions de touristes qui s’y rendent
On estime que 4000 à 6000 tonnes d’écran total sont libérées chaque année dans les zones de récifs tropicales par les 78 millions de touristes qui s’y rendent  En raison de son faible coût, l’huile de palme est, depuis quelques années, très utilisée dans l’alimentation: elle est présente dans 1 produit alimentaire empaqueté sur deux vendus en Europe (chips, biscuits, crème glacée, etc.). Or, la plantation de palmiers est à l’origine de déforestation, notamment en Indonésie. Dans ce pays, 3 millions d’hectares de forêt tropicale ont été détruits à cet effet entre 1990 et 2005 et le gouvernement prévoit un plan d’expansion des plantations de palmiers à huile de 14 millions d’hectares. La conversion des forêts en palmiers à huile a montré une perte de 80 à 100% des espèces de mammifères (dont l’orang-outan), reptiles et d’oiseaux dans ces zones
En raison de son faible coût, l’huile de palme est, depuis quelques années, très utilisée dans l’alimentation: elle est présente dans 1 produit alimentaire empaqueté sur deux vendus en Europe (chips, biscuits, crème glacée, etc.). Or, la plantation de palmiers est à l’origine de déforestation, notamment en Indonésie. Dans ce pays, 3 millions d’hectares de forêt tropicale ont été détruits à cet effet entre 1990 et 2005 et le gouvernement prévoit un plan d’expansion des plantations de palmiers à huile de 14 millions d’hectares. La conversion des forêts en palmiers à huile a montré une perte de 80 à 100% des espèces de mammifères (dont l’orang-outan), reptiles et d’oiseaux dans ces zones  Les animaux se nourrissent d’aliments (céréales, petits animaux, etc.) contenant différents polluants. Au fil du temps, ces derniers s’accumulent dans l’organisme de l’animal et en particulier dans les graisses (phénomène de bioaccumulation). Ainsi, une étude de 2010 a révélé la présence de nombreux pesticides et de PCB dans du saumon et du steak haché achetés dans des supermarchés de la région parisienne
Les animaux se nourrissent d’aliments (céréales, petits animaux, etc.) contenant différents polluants. Au fil du temps, ces derniers s’accumulent dans l’organisme de l’animal et en particulier dans les graisses (phénomène de bioaccumulation). Ainsi, une étude de 2010 a révélé la présence de nombreux pesticides et de PCB dans du saumon et du steak haché achetés dans des supermarchés de la région parisienne  Tout comme les fruits et légumes, le riz peut contenir différents polluants tels que des pesticides, en particulier s’il est issu d’une agriculture intensive classique (non « bio »). Ainsi, une étude de 2010 a révélé la présence d’isoprothiolane et de tricyclazole, 2 pesticides interdits d’usage en Europe, dans du riz acheté dans des supermarchés de la région parisienne
Tout comme les fruits et légumes, le riz peut contenir différents polluants tels que des pesticides, en particulier s’il est issu d’une agriculture intensive classique (non « bio »). Ainsi, une étude de 2010 a révélé la présence d’isoprothiolane et de tricyclazole, 2 pesticides interdits d’usage en Europe, dans du riz acheté dans des supermarchés de la région parisienne  L’eau du robinet est globalement de bonne qualité en France et les normes en vigueur sont généralement respectées
L’eau du robinet est globalement de bonne qualité en France et les normes en vigueur sont généralement respectées  Les fruits et légumes issus de l’agriculture intensive « classique » (c’est à dire non « bio ») contiennent des mélanges à faibles doses de substances chimiques classées, par les instances officielles, cancérogènes certaines, probables ou possibles ou soupçonnées d’être perturbatrices du système endocrinien. C’est ce qu’illustre notamment une étude de 2010 qui a révélé la présence de nombreux pesticides dans des produits achetés dans des supermarchés de la région parisienne
Les fruits et légumes issus de l’agriculture intensive « classique » (c’est à dire non « bio ») contiennent des mélanges à faibles doses de substances chimiques classées, par les instances officielles, cancérogènes certaines, probables ou possibles ou soupçonnées d’être perturbatrices du système endocrinien. C’est ce qu’illustre notamment une étude de 2010 qui a révélé la présence de nombreux pesticides dans des produits achetés dans des supermarchés de la région parisienne  Le lave-vaisselle est généralement moins consommateur en eau (12 L) que le lavage à la main qui dépend beaucoup du manipulateur (10 à 50 L)
Le lave-vaisselle est généralement moins consommateur en eau (12 L) que le lavage à la main qui dépend beaucoup du manipulateur (10 à 50 L)  Le liquide vaisselle est un détergent composé d’agents nettoyants appelés tensioactifs, mais aussi de colorants, conservateurs et parfums de synthèse. Bien que les tensioactifs ont l’obligation d’être biodégradables à 90%
Le liquide vaisselle est un détergent composé d’agents nettoyants appelés tensioactifs, mais aussi de colorants, conservateurs et parfums de synthèse. Bien que les tensioactifs ont l’obligation d’être biodégradables à 90%  Les composés perfluorés (PFC), tels que le téflon, ont la propriété de repousser l’eau, les matières grasses et la poussière. Ils sont ainsi utilisés comme antiadhésif dans de nombreuses poêles et casseroles. Les PFC sont persistants et s’accumulent dans les êtres vivants: certaines études ont révélé la présence de certains PFC dans les cours d’eau et les poissons (dans le foie notamment) ainsi que dans le sang humain
Les composés perfluorés (PFC), tels que le téflon, ont la propriété de repousser l’eau, les matières grasses et la poussière. Ils sont ainsi utilisés comme antiadhésif dans de nombreuses poêles et casseroles. Les PFC sont persistants et s’accumulent dans les êtres vivants: certaines études ont révélé la présence de certains PFC dans les cours d’eau et les poissons (dans le foie notamment) ainsi que dans le sang humain  3,8 millions de tonnes de bisphénol A (BPA) ont été produits en 2006
3,8 millions de tonnes de bisphénol A (BPA) ont été produits en 2006  Ces bouteilles contiennent notamment des phtalates, produits chimiques utilisés en tant que plastifiants et qui font partie de la famille des
Ces bouteilles contiennent notamment des phtalates, produits chimiques utilisés en tant que plastifiants et qui font partie de la famille des
6 commentaires
Houda
Très bon article merci énormément pour vos efforts
AYOUNE
Excellent article ! Illustrations remarquables.
Ping :
Darine Abada
Excellent article , très intéressant!
Bibi bi
Tralalero Tralala
John Doe
Bonjour à la L2 SIAS, très bonne article